0 68607 68615 68621 68625 68631 68633 68637 68643 68645 68651 68657 68661 68663 68667 68673 68675 68681 68685 68687 68691 68693 68697 68699 68701 68702 68703 68705 68706 68707 68709 68711 68715 68717 68721 68723 68727 68733 68735 68741 68745 68747 68751 68757 68763 68765 68771 68775 68777 68783 68787 68793 68801 203614

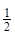 O2(g)=H2O(l)
ΔH3= ─285.8 kJ?mol-1
O2(g)=H2O(l)
ΔH3= ─285.8 kJ?mol-1 C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。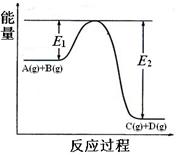

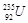 是重要的核工业原料,在自然界的含量很低,它的浓缩一直为国际社会所关注。下列有关
是重要的核工业原料,在自然界的含量很低,它的浓缩一直为国际社会所关注。下列有关 为U的两种核素 D.
为U的两种核素 D.