0 68478 68486 68492 68496 68502 68504 68508 68514 68516 68522 68528 68532 68534 68538 68544 68546 68552 68556 68558 68562 68564 68568 68570 68572 68573 68574 68576 68577 68578 68580 68582 68586 68588 68592 68594 68598 68604 68606 68612 68616 68618 68622 68628 68634 68636 68642 68646 68648 68654 68658 68664 68672 203614
 Z(g)达到平衡,正反应速率随时间的变化如图所示,下列叙述不正确的是( )
Z(g)达到平衡,正反应速率随时间的变化如图所示,下列叙述不正确的是( )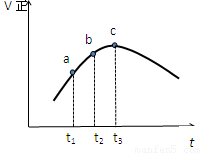
 xC(g)+2D(g)。若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L?min),请填写下列空白:
xC(g)+2D(g)。若经5min后反应达到平衡状态,容器内的压强变小,并知D的平均反应速率为0.2mol/(L?min),请填写下列空白:
 2AE2(g)已达到平衡状态的是 (填代号)
2AE2(g)已达到平衡状态的是 (填代号)