资料:(1)草酸亚铁晶体(FeC2O4·2H2O)呈淡黄色;(2)KMnO4在酸性条件的还原产物为Mn2+。某课题组为探究草酸亚铁晶体的化学性质,进行了一系列实验探究。
(1)向盛有草酸亚铁晶体的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现溶液颜色逐渐变为棕黄色,并检测到CO2生成。这说明草酸亚铁晶体具有 (填“氧化性”、“还原性”或“碱性”)。若反应中消耗1 mol FeC2O4·2H2O,则参加反应的KMnO4为 ______mol。
(2)资料表明:在密闭容器中加热到一定温度时,草酸亚铁晶体可完全分解,生成几种氧化物,残留物为黑色固体。课题组根据课本上所介绍的铁的氧化物的性质,对黑色固体的组成提出如下假设,请你完成假设二和假设三:
假设一:全部是FeO;假设二: ;假设三:
(3)为验证上述假设一是否成立,课题组进行如下研究。
【定性研究】请你完成下表中内容。
|
实验步骤(不要求具体的操作过程) |
预期实验现象和结论 |
|
取少量黑色固体, |
|
【定量研究】课题组在文献中查阅到,FeC2O4·2H2O受热分解时,固体质量随温度变化的曲线如下图所示,写出加热到400℃时,FeC2O4·2H2O晶体受热分解的化学方程式为: 。
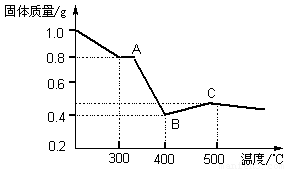
根据图象,如有1.0 g草酸亚铁晶体在坩埚中敞口充分加热,最终残留黑色固体的质量大于0.4 g。某同学由此得出结论:假设一不成立。你是否同意该同学的结论 (填“同意”或“不同意”),并简述理由 。
某酸HX稀溶液和某碱YOH稀溶液的物质的量浓度相等,两溶液混合后,下表各组关系可能合理的是
|
编号 |
HX |
YOH |
溶液体积 |
粒子浓度 |
|
① |
强酸 |
强碱 |
V(HX)= V (YOH) |
c(HX) + c(X-) = c(Y+) |
|
② |
弱酸 |
弱碱 |
V(HX)<V(YOH) |
c(X-) < c(Y+) |
|
③ |
强酸 |
强碱 |
V(HX)= V(YOH) |
c(H+)>c(YOH) + c(OH-) |
|
④ |
弱酸 |
弱碱 |
V(HX)>V(YOH) |
c(Y+) + c(H+) = c(X-) + c(OH-) |
A.①② B.②③ C.②④ D.③④
X、Y、Z、T、W五种元素的性质或原子结构如下表:
|
元素 |
元素性质或原子结构 |
|
X |
原子的最外层电子数是次外层电子数的2倍 |
|
Y |
常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
|
Z |
基态原子最外层电子排布式为(n+1)sn(n+1)pn+2 |
|
T |
与Z同周期,元素最高价是+7价 |
|
W |
原子序数为Y、T元素之和,不锈钢中含有该元素 |
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是_______;W元素基态原子电子排布式为________________________。
(2)元素Z与元素T相比,非金属性较强的是_______(用元素符号表示),下列表述中能证明这一事实的是______________。
A.常温下Z的单质和T的单质状态不同
B.T的氢化物比Z的氢化物稳定
C.一定条件下Z和T的单质都能与氢氧化钠溶液反应
D.T的电负性比Z大
(3)常见溶剂XZ2的分子中,含有的 键与π键个数比为_______,它所形成的晶体类型为_______;Y的常见氢化物易液化的主要原因是______________
键与π键个数比为_______,它所形成的晶体类型为_______;Y的常见氢化物易液化的主要原因是______________
(4)①自然界常见的X元素含氧酸的钙盐和适量T的氢化物溶液反应时,每产生4. 4g 气体(不考虑气体溶解)放热a kJ,则该反应的热化学方程式为______________。
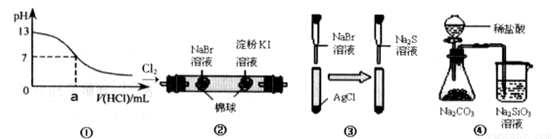
②上述反应至无气泡逸出后,取适量残留溶液,插入pH传感器并逐滴滴入碳酸钠溶液,测得PH变化 曲线如下图所示:

请用离子方程式表示BC段、CD段发生的反应:
BC段:__________________________________________;
CD段:__________________________________________。
 N2(g)+2CO2(g)
△H=-373.4kJ/mol
N2(g)+2CO2(g)
△H=-373.4kJ/mol
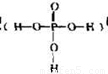 中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能跟D2O发生氢交换。由此可推断出H3PO2的分子结构是
中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能跟D2O发生氢交换。由此可推断出H3PO2的分子结构是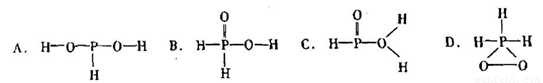

 表示(其中X、Y均不为H),且能发生银镜反应的物质有_______种,其中核磁共振氢谱有6个峰的物质结构简式为 (写出一种即可) ________________。
表示(其中X、Y均不为H),且能发生银镜反应的物质有_______种,其中核磁共振氢谱有6个峰的物质结构简式为 (写出一种即可) ________________。