0 68154 68162 68168 68172 68178 68180 68184 68190 68192 68198 68204 68208 68210 68214 68220 68222 68228 68232 68234 68238 68240 68244 68246 68248 68249 68250 68252 68253 68254 68256 68258 68262 68264 68268 68270 68274 68280 68282 68288 68292 68294 68298 68304 68310 68312 68318 68322 68324 68330 68334 68340 68348 203614
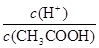 值增大
值增大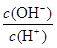 =1×10-8,则该溶液中由水电离出的c(H+)=1×10-11mol/L
=1×10-8,则该溶液中由水电离出的c(H+)=1×10-11mol/L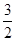 O2(g)=CO2(g)+2H2O(l)
△H=-764.5kJ/mol
O2(g)=CO2(g)+2H2O(l)
△H=-764.5kJ/mol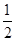 O2(g)=CO2(g) △H=-283.0kJ/mol
O2(g)=CO2(g) △H=-283.0kJ/mol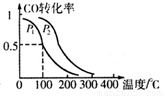 。
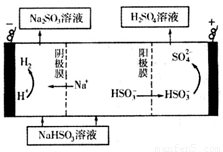
。


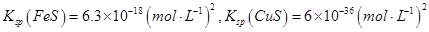

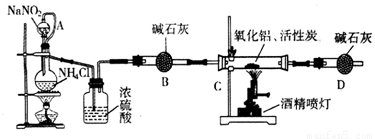
 。
。

