已知七种短周期元素a~g的有关信息如下表所示:
|
元素编号 |
a |
b |
c |
d |
e |
f |
g |
|
原子半径 / nm |
0.037 |
0.074 |
0.082 |
0.102 |
0.143 |
0.152 |
0.186 |
|
最高化合价或最低化合价 |
+1 |
-2 |
+3 |
-2 |
+3 |
+1 |
+1 |
下列推断正确的是
A.简单离子的离子半径:g < e
B.氢化物的稳定性强弱:b > d
C.元素e的氧化物是两性氧化物
D.元素a与元素d形成的化合物属于离子化合物
回收再利用锗产品加工废料,是生产GeO2的重要途径,其流程如下图:

(1)Ge2+与氧化剂H2O2反应生成Ge4+,写出该反应的离子方程式 。
(2)蒸馏可获得沸点较低的GeCl4,在此过程中加入浓盐酸的原因是 。实验室蒸馏操作时常用的玻璃仪器有:酒精灯、蒸馏烧瓶、 、 、接收管、锥形瓶等。
(3)GeCl4水解生成GeO2·nH2O,此过程用化学方程式可表示为 。
温度对GeCl4的水解率产生的影响如图1所示,其原因是 。 为控制最佳的反应温度,实验时可采取的措施为 (填序号)。

A.用冰水混合物 B.49℃水浴 C.用冰盐水
(4)结合Ge在元素周期表中的位置及“对角线”法则,分析GeO2溶解率随pH 变化的原因 ,用离子方程式表示pH>8时GeO2溶解率增大可能发生的反应 。
|
pH |
4 |
5 |
6 |
7 |
8 |
9 |
|
溶解率/% |
47.60 |
32.53 |
11.19 |
5.27 |
1.96 |
8.85 |
漂白粉是一种常用的消毒剂。
(1)工业上生产漂白粉反应的化学方程式为:________________ __,漂白粉的有效成分为 。
(2)某探究小组从市场上购买了一袋包装破损的漂白粉,对该漂白粉的成分进行探究。根据下列试剂,设计实验方案,进行实验。请在答题卡上完成实验报告。
限选试剂:2mol·L-1NaOH溶液、2mol·L-1HCl溶液、2mol·L-1HNO3溶液、0.5mol·L-1BaCl2溶液、0.01mol·L-1AgNO3溶液、澄清石灰水、石蕊试液、酚酞试液、蒸馏水。
|
实验步骤 |
预期现象与结论 |
|
步骤1:取适量漂白粉溶于足量蒸馏水,充分搅拌,静置,过滤,得沉淀和滤液。 |
|
|
步骤2:向沉淀加入适量2mol·L-1HCl溶液,将产生的气体通入
|
现象:
结论: |
|
步骤3:取滤液分装A、B两支试管。向A试管,
|
现象:溶液先变红色,然后褪色。 结论:
|
|
步骤4:向B试管,
|
现象:产生白色沉淀。 结论: |
(3)探究小组为测定漂白粉中Ca(ClO)2的含量:称取漂白粉bg加水溶解后配制成100mL溶液,准确量取25.00mL于锥形瓶并加入足量盐酸和KI溶液,充分反应后,溶液中的游离碘用0.1000mol/L的Na2S2O3溶液滴定,滴定2次,平均消耗Na2S2O3溶液20.00mL。则该漂白粉中Ca(ClO)2的质量分数为_____________ _。(只列算式,不做运算,已知:Mr[Ca(ClO)2]=143 ;Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O,2Na2S2O3+I2=Na2S4O6+2NaI)
化学在日常生活中具有广泛的应用,下列应用中不涉及氧化还原反应原理的是
A.用明矾[KAl(SO4)2·12H2O]净水 B.海水中提取溴
C.交警用CrO3检验司机是否酒后驾驶 D.医务室用双氧水消毒
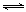 2Fe2++I2设计成如图所示的原电池。下列判断不正确的是
2Fe2++I2设计成如图所示的原电池。下列判断不正确的是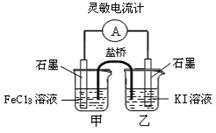

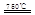 CaO+2HBr ②2HBr+Hg
CaO+2HBr ②2HBr+Hg HgBr2+H2
HgBr2+H2 _____ + ④2HgO
_____ + ④2HgO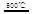 2Hg+O2↑
2Hg+O2↑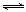 CO2(g)+H2(g) △H<0
CO2(g)+H2(g) △H<0