相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:X2(g)+3Y2(g)?2XY3(g);△H=-92.6kJ?mol-1,实验测得反应起始时、达到平衡状态时的有关数据如下表所示,不正确的是( )
A.达平衡时,两个容器中XY3的物质的量浓度均为2mol?L-1
B.容器①、②中反应的平衡常数相等
C.容器②中反应达到平衡状态时放出23.15× kJ的热量
kJ的热量
D.若容器①体积为0.20L,则反应达到平衡状态时放出的热量大于23.15kJ
| 容器 编号 | 起始时各物质物质的量/mol | 平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 放热Q1=23.15kJ | |
| ② | 0.6 | 1.8 | 0.8 | Q2 |
A.达平衡时,两个容器中XY3的物质的量浓度均为2mol?L-1
B.容器①、②中反应的平衡常数相等
C.容器②中反应达到平衡状态时放出23.15×
 kJ的热量
kJ的热量D.若容器①体积为0.20L,则反应达到平衡状态时放出的热量大于23.15kJ
硫酸亚铁是比较重要的亚铁盐,在农业上用作农药,主治小麦黑穗病,在工业上用于染色、制造蓝黑墨水和木材防腐、除草剂等.
(1)实验室条件下用铁粉和稀硫酸制取少量硫酸亚铁溶液,为防止其变质,应在该溶液中应加入适量______.
(2)新制的绿矾晶体是浅绿色的,但在空气中极易变成黄色或铁锈色的碱式硫酸铁[Fe(OH)SO4],写出该反应的化学方程式:______.
(3)已知FeSO4在不同条件下分解得到的产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2.某研究小组探究在酒精喷灯加热条件下FeSO4分解的气体产物.已知SO3的熔点是16.8°C,沸点是44.8°C.
①装置II的试管中不装任何试剂,其作用是______,试管浸泡在50℃的热水浴中,目的是______.
②装置III和装置IV的作用是探究本实验气体产物成分.请完成实验设计,填写检验试剂、预期现象与结论.
限选试剂:3mol.L-1.H2S04、6mol.L-l NaOH、0.5mol.L -1 BaCl2、O.5mol.L-1Ba(NO3)2、0.01mol.L-1 酸性 KMnO4 溶液、0.0l mol.L-1 溴水.

③装置V的作用是防止尾气污染环境,烧杯中应加入的试剂是______.
④如何检验装置Ⅰ中固体完全分解后生成固体产物有无FeO?写出步骤、现象及结论:______.
(1)实验室条件下用铁粉和稀硫酸制取少量硫酸亚铁溶液,为防止其变质,应在该溶液中应加入适量______.
(2)新制的绿矾晶体是浅绿色的,但在空气中极易变成黄色或铁锈色的碱式硫酸铁[Fe(OH)SO4],写出该反应的化学方程式:______.
(3)已知FeSO4在不同条件下分解得到的产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2.某研究小组探究在酒精喷灯加热条件下FeSO4分解的气体产物.已知SO3的熔点是16.8°C,沸点是44.8°C.
①装置II的试管中不装任何试剂,其作用是______,试管浸泡在50℃的热水浴中,目的是______.
②装置III和装置IV的作用是探究本实验气体产物成分.请完成实验设计,填写检验试剂、预期现象与结论.
限选试剂:3mol.L-1.H2S04、6mol.L-l NaOH、0.5mol.L -1 BaCl2、O.5mol.L-1Ba(NO3)2、0.01mol.L-1 酸性 KMnO4 溶液、0.0l mol.L-1 溴水.

| 检验试剂 | 预期现象与结论 |
| 装置III的试管中加入足量______. | 产生大量白色沉淀,证明气体产物中含有SO3. |
| 装置IV的试管中加入足量______. | ______ ______. |
④如何检验装置Ⅰ中固体完全分解后生成固体产物有无FeO?写出步骤、现象及结论:______.
氧气是化工生产的重要原料,很多金属和非金属都能和氧气直接作用.
(1)第二周期某种元素形成的氧化物分子中,既含有σ键又含有π键且二者数目相同的物质的结构式为______,其中心原子杂化方式为______.氧元素与氟元素能形成OF2分子,该分子的空间构型为______.氮元素的电负性______(填“>”、“=”或“<”)氧,主要原因是______.
(2)氧元素和过渡元素可形成多种价态的金属氧化物,如Cr2O3、Fe2O3、V2O5.基态铬原子外围电子排布式为______.核电荷数比Fe大1的元素在元素周期表中的位置为第______周期______族.
(3)四种同主族元素的氧化物晶体的晶格能数据如下表:
四种氧化物的共熔物冷却时,首先析出的是______.根据表中数据,说明影响上表中晶格能大小的主要因素______.
(4)某种由氧和钾元素形成的化合物,其晶胞结构如右图所示,该晶体的化学式为______.

0 67852 67860 67866 67870 67876 67878 67882 67888 67890 67896 67902 67906 67908 67912 67918 67920 67926 67930 67932 67936 67938 67942 67944 67946 67947 67948 67950 67951 67952 67954 67956 67960 67962 67966 67968 67972 67978 67980 67986 67990 67992 67996 68002 68008 68010 68016 68020 68022 68028 68032 68038 68046 203614
(1)第二周期某种元素形成的氧化物分子中,既含有σ键又含有π键且二者数目相同的物质的结构式为______,其中心原子杂化方式为______.氧元素与氟元素能形成OF2分子,该分子的空间构型为______.氮元素的电负性______(填“>”、“=”或“<”)氧,主要原因是______.
(2)氧元素和过渡元素可形成多种价态的金属氧化物,如Cr2O3、Fe2O3、V2O5.基态铬原子外围电子排布式为______.核电荷数比Fe大1的元素在元素周期表中的位置为第______周期______族.
(3)四种同主族元素的氧化物晶体的晶格能数据如下表:
| 氧化物 | MgO | CaO | SrO | BaO |
| 晶格能/kJ?mol-1 | 3791 | 3410 | 3223 | 3054 |
(4)某种由氧和钾元素形成的化合物,其晶胞结构如右图所示,该晶体的化学式为______.


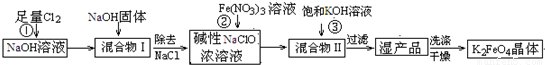
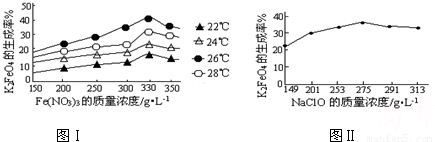
 4Fe(OH)3+8OH-+3O2↑.在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用______溶液(填序号).
4Fe(OH)3+8OH-+3O2↑.在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用______溶液(填序号).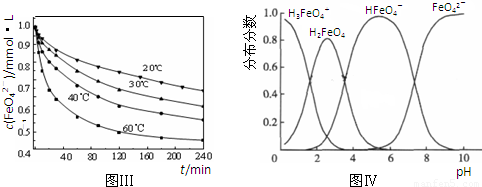
 ,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂.
,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂.