Ⅰ以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工业.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g) CO(g)+H2(g)△H=+131.3kJ?mol-1,
CO(g)+H2(g)△H=+131.3kJ?mol-1,
该反应在常温下 自发进行(填“能”与“不能”);在一体积为2L的密闭容器中,加入1molC和2mol H2O(g),达平衡时H2O的转化率为20%,请计算此时的平衡常数
(2)目前工业上有一种方法是用CO与H2反应来生产甲醇.
已知生成气态甲醇,CO里面含C≡O.请写出该反应的热化学方程式为
(3)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:
N2(g)+3H2(g) 2NH3(g)△H=-92.4kJ/mol
2NH3(g)△H=-92.4kJ/mol
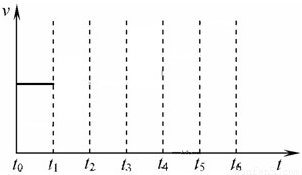
在一体积不变的容器中,当合成氨反应达到平衡后,在t1时升高温度,t2重新达到平衡,t3时充入氮气,t4时重新达到平衡,t5时移去一部分产物,t6时又达到平衡,请在下面的反应速率与时间关系图中画出t1到t5逆反应速率、t5到t6正反应速率的变化情况.
(4)氢气可用于生产燃料电池,丙烷气体也可以.美国科学家成功开发便携式固体氧化物燃料电池,它以丙烷气体为燃料,一极通入空气,另一极通入丙烷气体,电解质是固态氧化物,在熔融状态下能传导O2-.则通丙烷的电极发生的电极反应为
Ⅱ沉淀物并非绝对不溶,且在水及各种不同的溶液中溶解度有所不同,同离子效应、络合物的形成等都会使沉淀物的溶解度有所改变.已知AgCl+Cl-=[AgCl2]-,如图是某温度下AgCl在NaCl溶液中的溶解情况.由以上信息可知:
(1)由图知该温度下AgCl的溶度积常数为 .
(2)AgCl在NaCl溶液中的溶解出现如图所示情况(先变小后变大)的原因是: .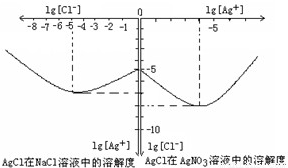
0 67827 67835 67841 67845 67851 67853 67857 67863 67865 67871 67877 67881 67883 67887 67893 67895 67901 67905 67907 67911 67913 67917 67919 67921 67922 67923 67925 67926 67927 67929 67931 67935 67937 67941 67943 67947 67953 67955 67961 67965 67967 67971 67977 67983 67985 67991 67995 67997 68003 68007 68013 68021 203614
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)
 CO(g)+H2(g)△H=+131.3kJ?mol-1,
CO(g)+H2(g)△H=+131.3kJ?mol-1,该反应在常温下 自发进行(填“能”与“不能”);在一体积为2L的密闭容器中,加入1molC和2mol H2O(g),达平衡时H2O的转化率为20%,请计算此时的平衡常数
(2)目前工业上有一种方法是用CO与H2反应来生产甲醇.
| 化学键 | C-O | C-H | H-H | C≡O | O-H |
| 键能 kg/mol-1 | 358 | 413 | 436 | 1072 | 463 |
(3)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:
N2(g)+3H2(g)
 2NH3(g)△H=-92.4kJ/mol
2NH3(g)△H=-92.4kJ/mol在一体积不变的容器中,当合成氨反应达到平衡后,在t1时升高温度,t2重新达到平衡,t3时充入氮气,t4时重新达到平衡,t5时移去一部分产物,t6时又达到平衡,请在下面的反应速率与时间关系图中画出t1到t5逆反应速率、t5到t6正反应速率的变化情况.
(4)氢气可用于生产燃料电池,丙烷气体也可以.美国科学家成功开发便携式固体氧化物燃料电池,它以丙烷气体为燃料,一极通入空气,另一极通入丙烷气体,电解质是固态氧化物,在熔融状态下能传导O2-.则通丙烷的电极发生的电极反应为
Ⅱ沉淀物并非绝对不溶,且在水及各种不同的溶液中溶解度有所不同,同离子效应、络合物的形成等都会使沉淀物的溶解度有所改变.已知AgCl+Cl-=[AgCl2]-,如图是某温度下AgCl在NaCl溶液中的溶解情况.由以上信息可知:
(1)由图知该温度下AgCl的溶度积常数为 .
(2)AgCl在NaCl溶液中的溶解出现如图所示情况(先变小后变大)的原因是: .


 ;六种元素在周期表中的位置关系是:A、B同主族,C、D也同主族;C、E相邻,B、F也相邻.
;六种元素在周期表中的位置关系是:A、B同主族,C、D也同主族;C、E相邻,B、F也相邻.



 Si+2CO↑的反应中,每当有1mol气体生成,就有4N4个电子转移
Si+2CO↑的反应中,每当有1mol气体生成,就有4N4个电子转移 )>0.4mol?L-1
)>0.4mol?L-1
 (aq)+H2O(l)△H=-57.3kJ?mol-1
(aq)+H2O(l)△H=-57.3kJ?mol-1 +Ba2++2OH-=BaSO4↓+2H2O
+Ba2++2OH-=BaSO4↓+2H2O