实验室制备纯碱的主要步骤是:①将配制好的饱和NaCl溶液倒入烧杯中加热,控制温
度在30--35℃,搅拌下分批加入研细的NH4HC03固体,②加料完毕后,继续保温30分钟,③静置、过滤得NaHC03晶体.④用少量蒸馏水洗涤除去杂质,抽干后,转入蒸发皿中,灼烧,制得Na2C03固体.
四种盐在不回温度下的溶解度(g/l00g水)表
①>35℃NH4HC03会有分解
请回答:
(1)反应温度控制在30-35℃,是因为______;为控制此温度范围,采取的加热方法为______.
(2)加料完毕后,继续保温30分钟,目的是______;静置后只析出NaHCO3品体的原因是______.
(3)洗涤NaHC03晶体的操作是______.
(4)过滤所得的母液中含有的溶质______(以化学式表示).
(5)写出本实验中制备纯碱的有关化学方程式______.
(6)测试纯碱产品中NaHC03含量的方法是:准确称取纯碱样品W g,放入锥形瓶中加蒸馏水溶解,加1-2滴酚酞指示剂,用物质的量浓度为c (mol/L)的HCl溶液滴定至溶液由红色到无色,所用HCl溶液体积为V1 mL,再加1-2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,所用HC1溶液总体积为V2mL,写出纯碱样品中NaHCO3质量分数的计算式:______.
度在30--35℃,搅拌下分批加入研细的NH4HC03固体,②加料完毕后,继续保温30分钟,③静置、过滤得NaHC03晶体.④用少量蒸馏水洗涤除去杂质,抽干后,转入蒸发皿中,灼烧,制得Na2C03固体.
四种盐在不回温度下的溶解度(g/l00g水)表
 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | -① | |||
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
请回答:
(1)反应温度控制在30-35℃,是因为______;为控制此温度范围,采取的加热方法为______.
(2)加料完毕后,继续保温30分钟,目的是______;静置后只析出NaHCO3品体的原因是______.
(3)洗涤NaHC03晶体的操作是______.
(4)过滤所得的母液中含有的溶质______(以化学式表示).
(5)写出本实验中制备纯碱的有关化学方程式______.
(6)测试纯碱产品中NaHC03含量的方法是:准确称取纯碱样品W g,放入锥形瓶中加蒸馏水溶解,加1-2滴酚酞指示剂,用物质的量浓度为c (mol/L)的HCl溶液滴定至溶液由红色到无色,所用HCl溶液体积为V1 mL,再加1-2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,所用HC1溶液总体积为V2mL,写出纯碱样品中NaHCO3质量分数的计算式:______.
(1)下表为某温度和压强下,密闭容器中SO2氧化为SO3反应在不同时间各物质的浓度(mol/L)
试画出V(SO3)-t图.

(2)工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤.压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2:7%,O2:11%,N2:82%):
①如何利用表中数据推断SO2的氧化反应的热效应?______.
②在400一500℃时,SO2的催化氧化采用常压而不是高压,主要原因是:______.
③工业制硫酸所产生的尾气含有SO2、微量的SO3和酸雾.为了保护环境将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式:______.
④能用于测定硫酸尾气中SO2含量的是______.(填字母)
A.NaOH溶液、酚酞试液
B.KMnO4溶液、稀H2SO4
C.碘水、淀粉溶液
D.氨水、酚酞试液
⑤某温度下,SO2氧化为SO3在10L的密闭容器中进行,开始向容器加入4.0mol SO2和10.0mo1O2,当反应达到平衡时,混合气体为13.0mol,则SO2的转化率为______,该温度反应的平衡常数______.
| 时间(min) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| SO2 | 10 | 7 | 5 | 3.5 | 2 | 1 | 1 | 1 |
| O2 | 5 | 3.5 | 2.5 | 1.75 | 1 | 0.5 | 0.5 | 0.5 |
| SO3 | 3 | 5 | 6.5 | 8 | 9 | 9 | 9 |

(2)工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤.压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2:7%,O2:11%,N2:82%):
| 压强/MPa 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2% | 99.6% | 99.7% | 99.9% |
| 500 | 93.5% | 96.9% | 97.8% | 99.3% |
| 600 | 73.7% | 85.8% | 89.5% | 96.4% |
②在400一500℃时,SO2的催化氧化采用常压而不是高压,主要原因是:______.
③工业制硫酸所产生的尾气含有SO2、微量的SO3和酸雾.为了保护环境将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式:______.
④能用于测定硫酸尾气中SO2含量的是______.(填字母)
A.NaOH溶液、酚酞试液
B.KMnO4溶液、稀H2SO4
C.碘水、淀粉溶液
D.氨水、酚酞试液
⑤某温度下,SO2氧化为SO3在10L的密闭容器中进行,开始向容器加入4.0mol SO2和10.0mo1O2,当反应达到平衡时,混合气体为13.0mol,则SO2的转化率为______,该温度反应的平衡常数______.
己知羰基化合物与饱和NaHSO3溶液可以发生以下反应:

(1)羰基化合物和饱和NaHSO3的反应速率如下:
可见,取代基对羰基化合物和NaHSO3反应的影响有(写出3条即可)
①______,
②______,
③______.
(2)利用以上可逆反应可以分离醛和酮的混合物,请写出能使醛与NaHSO3生成的沉淀重新溶解的试剂的化学式______(写出2种,属于不同类别的物质)
(3)检验甲基酮(RCOCH3)通常用到下列2步反应来生成难溶于水的氯仿.
(CH3)2CHCOCH3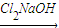 (CH3)2CHCOCCl3
(CH3)2CHCOCCl3 A+HCCl3↓
A+HCCl3↓
①写出第一步反应的化学方程式______;
②写出A的结构简式______;
(4)苯甲醛与在浓NaOH溶液反应生成苯甲酸钠和苯甲醇,此反应的类型是______;分离该反应产物的操作名称是______.
0 67754 67762 67768 67772 67778 67780 67784 67790 67792 67798 67804 67808 67810 67814 67820 67822 67828 67832 67834 67838 67840 67844 67846 67848 67849 67850 67852 67853 67854 67856 67858 67862 67864 67868 67870 67874 67880 67882 67888 67892 67894 67898 67904 67910 67912 67918 67922 67924 67930 67934 67940 67948 203614

(1)羰基化合物和饱和NaHSO3的反应速率如下:
| 羰基化合物 | CH3CHO | CH3COCH3 | C2H5COCH3 | CH3CH2CH2COCH3 |
| 产率(1小时内) | 88.7 | 56.2 | 36.4 | 23.4 |
| 羰基化合物 | (CH3)2CHCOCH3 | (CH3)3CCOCH3 | C2H5COC2H5 | C6H5COCH3 |
| 产率(1小时内) | 12.3 | 5.6 | 2 | 1 |
①______,
②______,
③______.
(2)利用以上可逆反应可以分离醛和酮的混合物,请写出能使醛与NaHSO3生成的沉淀重新溶解的试剂的化学式______(写出2种,属于不同类别的物质)
(3)检验甲基酮(RCOCH3)通常用到下列2步反应来生成难溶于水的氯仿.
(CH3)2CHCOCH3
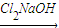 (CH3)2CHCOCCl3
(CH3)2CHCOCCl3 A+HCCl3↓
A+HCCl3↓①写出第一步反应的化学方程式______;
②写出A的结构简式______;
(4)苯甲醛与在浓NaOH溶液反应生成苯甲酸钠和苯甲醇,此反应的类型是______;分离该反应产物的操作名称是______.
 +c(OH-)=c(H+)+c(CH2COOH)
+c(OH-)=c(H+)+c(CH2COOH) >c(OH-)>c(H+)
>c(OH-)>c(H+)




 、
、 、HClO K=2.9×10-8
、HClO K=2.9×10-8



