甲醇是一种很好的燃料,工业上用CH4和H2O为原料,通过下述反应Ⅰ和Ⅱ来制备甲醇.
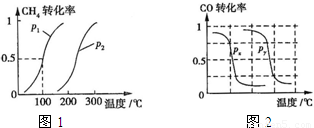
(1)将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),在一定条件下发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g)…I.CH4的转化率与温度、压强的关系如图.
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为______.
②图中的P1______P2(填“<”、“>”或“=”),100℃时平衡常数为______.
③该反应的△H______0(填“<”、“>”或“=”).
(2)在压强为0.1MPa条件下,将a mol CO与3amol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g)?CH3OH(g)△H<0
Ⅱ.
①若容器容积不变,下列措施可增加甲醇产率的是______.
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1mol CO和3mol H2
②为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.
A.则上表中剩余的实验条件数据:a=______、b=______.
B.根据反应Ⅱ的特点,右上图是在压强分别为0.1MPa和5MPa下CO的转化率随温度变化的曲线图,请指明图中的压强Px=______MPa.
0 67731 67739 67745 67749 67755 67757 67761 67767 67769 67775 67781 67785 67787 67791 67797 67799 67805 67809 67811 67815 67817 67821 67823 67825 67826 67827 67829 67830 67831 67833 67835 67839 67841 67845 67847 67851 67857 67859 67865 67869 67871 67875 67881 67887 67889 67895 67899 67901 67907 67911 67917 67925 203614
(1)将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),在一定条件下发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g)…I.CH4的转化率与温度、压强的关系如图.
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为______.
②图中的P1______P2(填“<”、“>”或“=”),100℃时平衡常数为______.
③该反应的△H______0(填“<”、“>”或“=”).
(2)在压强为0.1MPa条件下,将a mol CO与3amol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g)?CH3OH(g)△H<0
Ⅱ.
①若容器容积不变,下列措施可增加甲醇产率的是______.
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1mol CO和3mol H2
②为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.
| 实验编号 | T(℃) | n(CO)/n(H2) | p(MPa) |
| l | 150 |  | 0.1 |
| 2 | n |  | 5 |
| 3 | 350 | m | 5 |
B.根据反应Ⅱ的特点,右上图是在压强分别为0.1MPa和5MPa下CO的转化率随温度变化的曲线图,请指明图中的压强Px=______MPa.

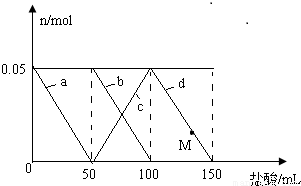 向含Na2CO3、Na[Al(OH)4]的混合溶液中逐滴加入150mL 1mol?L-1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法不正确的是( )
向含Na2CO3、Na[Al(OH)4]的混合溶液中逐滴加入150mL 1mol?L-1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法不正确的是( )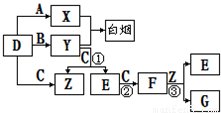
 ,而在潮湿空气中发生吸氧腐蚀是钢铁腐蚀的主要原因.
,而在潮湿空气中发生吸氧腐蚀是钢铁腐蚀的主要原因.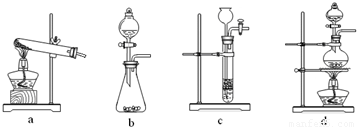
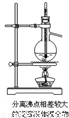
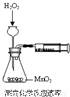
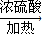 CO↑+CO2↑+H2O,下列装置中,可用作草酸分解制取气体的是______.(填字母)
CO↑+CO2↑+H2O,下列装置中,可用作草酸分解制取气体的是______.(填字母)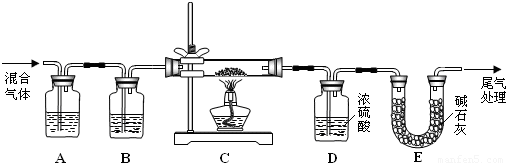
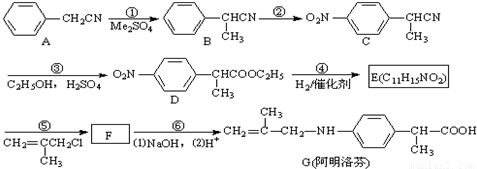
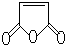 是合成某些药物的中间体.试设计合理方案由化合物
是合成某些药物的中间体.试设计合理方案由化合物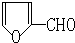 合成
合成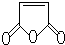 .
.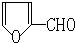 在400℃、金属氧化物条件下能发生脱羰基反应;
在400℃、金属氧化物条件下能发生脱羰基反应;