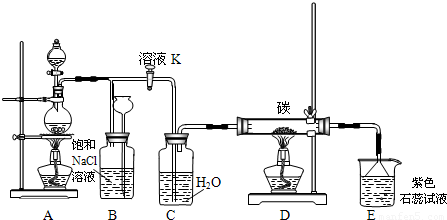
某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色.
(1)提出问题:Fe3+与Br2,谁的氧化性更强?
(2)猜想:①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是因为含有______(填化学式,下同)所致.
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是因为含有______(填化学式,下同)所致.
(3)设计实验并验证:丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并观察实验现象,证明了乙同学的观点是正确的.
供选用的试剂:a、酚酞试液 b、CCl4 c、无水酒精 d、KSCN溶液
请你在下表中写出丙同学选用的试剂及实验中观察到的现象(试剂填序号).
(4)结论:氧化性:Br2>Fe3+.故在足量的稀氯化亚铁溶液中加入1~2滴溴水,溶液呈黄色所发生反应的离子方程式为:______.
(5)实验后的思考:
①可以推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是(填离子符号)______;
②在100mL FeBr2溶液中通入2.24L Cl2(标准状况),溶液中的 的Br-被氧化为Br2,则原FeBr2溶液中FeBr2的物质的量浓度是:______.
的Br-被氧化为Br2,则原FeBr2溶液中FeBr2的物质的量浓度是:______.
0 67725 67733 67739 67743 67749 67751 67755 67761 67763 67769 67775 67779 67781 67785 67791 67793 67799 67803 67805 67809 67811 67815 67817 67819 67820 67821 67823 67824 67825 67827 67829 67833 67835 67839 67841 67845 67851 67853 67859 67863 67865 67869 67875 67881 67883 67889 67893 67895 67901 67905 67911 67919 203614
(1)提出问题:Fe3+与Br2,谁的氧化性更强?
(2)猜想:①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是因为含有______(填化学式,下同)所致.
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是因为含有______(填化学式,下同)所致.
(3)设计实验并验证:丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并观察实验现象,证明了乙同学的观点是正确的.
供选用的试剂:a、酚酞试液 b、CCl4 c、无水酒精 d、KSCN溶液
请你在下表中写出丙同学选用的试剂及实验中观察到的现象(试剂填序号).
| 试剂 | 实验现象 | |
| 方案1 | ______ | ______ |
| 方案2 | ______ | ______ |
(5)实验后的思考:
①可以推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是(填离子符号)______;
②在100mL FeBr2溶液中通入2.24L Cl2(标准状况),溶液中的
 的Br-被氧化为Br2,则原FeBr2溶液中FeBr2的物质的量浓度是:______.
的Br-被氧化为Br2,则原FeBr2溶液中FeBr2的物质的量浓度是:______.