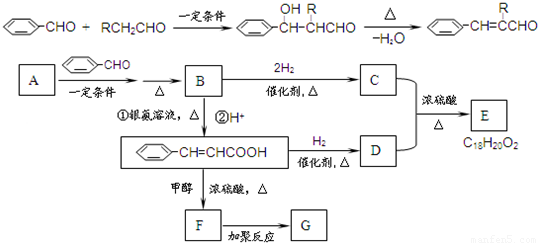
a、b、c、d是短周期元素,在周期表中的相对位置如图所示.c元素原子核外M层电子数是K层电子数的2倍.下列说法中,错误的是( )
A.原子半径:c<b
B.气态氢化物的稳定性:b>d
C.高温下,a单质可与c的氧化物发生置换反应
D.b的最高价氧化物对应的水化物中既含共价键又含离子键
| a | b |
| c | d |
A.原子半径:c<b
B.气态氢化物的稳定性:b>d
C.高温下,a单质可与c的氧化物发生置换反应
D.b的最高价氧化物对应的水化物中既含共价键又含离子键
苯乙烷(  -C2H5)可生产塑料单体苯乙烯(
-C2H5)可生产塑料单体苯乙烯( -CH=CH2),其原理反应是:
-CH=CH2),其原理反应是:
 -C2H5(g)
-C2H5(g) 
 -CH=CH2(g)+H2(g);△H=+125kJ?mol-1.某温度下,将0.40mol
-CH=CH2(g)+H2(g);△H=+125kJ?mol-1.某温度下,将0.40mol  -C2H5(g)充入2L真空密闭容器中发生反应,测定该容器内的物质,得到数据如下表:
-C2H5(g)充入2L真空密闭容器中发生反应,测定该容器内的物质,得到数据如下表:
(1)n1=______mol,计算该反应的平衡常数,K=______.
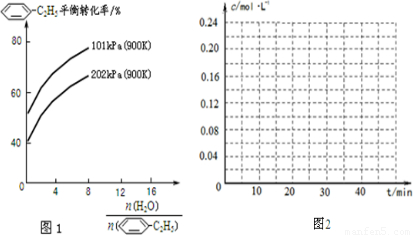
(2)工业上常以高温水蒸气作为反应体系的稀释剂(不参与反应). -C2H5(g)的平衡转化率与水蒸气的用量、体系总压强的关系如图1所示.当其它条件不变时,水蒸气的用量越大,平衡转化率将______(填“越大”、“越小”或“不变”),原因是______.
-C2H5(g)的平衡转化率与水蒸气的用量、体系总压强的关系如图1所示.当其它条件不变时,水蒸气的用量越大,平衡转化率将______(填“越大”、“越小”或“不变”),原因是______.
(3)副产物H2用做氢氧燃料电池.写出酸性条件下,该电池正极的电极反应式______.
(4)在相同条件下,若最初向该容器中充入 -CH=CH2(g)和H2(g),假设在40min时达到上述同样的平衡状态,请在图2中画出并标明该条件下
-CH=CH2(g)和H2(g),假设在40min时达到上述同样的平衡状态,请在图2中画出并标明该条件下  -C2H5(g)和
-C2H5(g)和 -CH=CH2(g)的浓度c随时间t变化的曲线______.
-CH=CH2(g)的浓度c随时间t变化的曲线______.
 -C2H5)可生产塑料单体苯乙烯(
-C2H5)可生产塑料单体苯乙烯( -CH=CH2),其原理反应是:
-CH=CH2),其原理反应是: -C2H5(g)
-C2H5(g) 
 -CH=CH2(g)+H2(g);△H=+125kJ?mol-1.某温度下,将0.40mol
-CH=CH2(g)+H2(g);△H=+125kJ?mol-1.某温度下,将0.40mol  -C2H5(g)充入2L真空密闭容器中发生反应,测定该容器内的物质,得到数据如下表:
-C2H5(g)充入2L真空密闭容器中发生反应,测定该容器内的物质,得到数据如下表:| 时间/min | 10 | 20 | 30 | 40 | |
n( -C2H5)/mol -C2H5)/mol | 0.40 | 0.30 | 0.26 | n2 | n3 |
n( -CH=CH2)/mol -CH=CH2)/mol | 0.00 | 0.10 | n1 | 0.16 | 0.16 |
(2)工业上常以高温水蒸气作为反应体系的稀释剂(不参与反应).
 -C2H5(g)的平衡转化率与水蒸气的用量、体系总压强的关系如图1所示.当其它条件不变时,水蒸气的用量越大,平衡转化率将______(填“越大”、“越小”或“不变”),原因是______.
-C2H5(g)的平衡转化率与水蒸气的用量、体系总压强的关系如图1所示.当其它条件不变时,水蒸气的用量越大,平衡转化率将______(填“越大”、“越小”或“不变”),原因是______.(3)副产物H2用做氢氧燃料电池.写出酸性条件下,该电池正极的电极反应式______.
(4)在相同条件下,若最初向该容器中充入
 -CH=CH2(g)和H2(g),假设在40min时达到上述同样的平衡状态,请在图2中画出并标明该条件下
-CH=CH2(g)和H2(g),假设在40min时达到上述同样的平衡状态,请在图2中画出并标明该条件下  -C2H5(g)和
-C2H5(g)和 -CH=CH2(g)的浓度c随时间t变化的曲线______.
-CH=CH2(g)的浓度c随时间t变化的曲线______.
钛(Ti)具有高强度和耐酸腐蚀性,是重要的工业原料.以金红石(主要成分为TiO2,含少量Fe2O3、SiO2)为原料可制取Ti.工业流程如下:

(1)粗TiCl4中含有少量FeCl3、SiCl4等,它们的部分性质如下:
从粗TiCl4中精制TiCl4的方法是______ A.用水溶解后,重结晶 B.蒸馏 C.用乙醚萃取后,分液
(2)写出金红石高温反应制取TiCl4的化学方程式______ TiCl4+2CO

(1)粗TiCl4中含有少量FeCl3、SiCl4等,它们的部分性质如下:
| 物质 | 沸点/°C | 在水中 | 在乙醚中 |
| TiCl4 | 136 | 强烈水解 | 易溶 |
| SiCl4 | 58 | 强烈水解 | 易溶 |
| FeCl3 | 303(升华) | 水解 | 易溶 |
(2)写出金红石高温反应制取TiCl4的化学方程式______ TiCl4+2CO
NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+=Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况.
(1)此消毒液可吸收空气中的CO2生成NaHCO3而变质.写出化学反应方程式______.
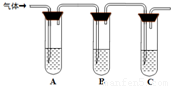
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出.通过以下装置检验气体的成分可以判断消毒液是否变质.
限选试剂:98%浓硫酸、1%品红溶液、1.0mol?L-1 KI-淀粉溶液、1.0mol?L-1NaOH、澄清石灰水、饱和NaCl溶液
请完成下列实验方案.
(3)用滴定法测定消毒液中NaClO的浓度.实验步骤如下:
①量取25.00mL消毒液放入锥形瓶中,加入过量的a mol?L-1Na2SO3溶液b mL;
②滴定分析.将c mol?L-1的酸性KMnO4溶液装入______(填酸式或碱式)滴定管中;KMnO4和剩余的Na2SO3发生反应.当溶液由无色变成浅红色,且保持半分钟内红色不退时,停止滴定,记录数据.重复滴定实验2次,平均消耗酸性KMnO4溶液v mL;
滴定过程中涉及的反应有:NaClO+Na2SO3=NaCl+Na2SO4;2KMnO4+5Na2SO3+3H2SO4=K2SO4+2MnSO4+5Na2SO4+3H2O.
③计算.消毒液中NaClO的浓度为______mol?L-1(用含a、b、c、v的代数式表示).
0 67720 67728 67734 67738 67744 67746 67750 67756 67758 67764 67770 67774 67776 67780 67786 67788 67794 67798 67800 67804 67806 67810 67812 67814 67815 67816 67818 67819 67820 67822 67824 67828 67830 67834 67836 67840 67846 67848 67854 67858 67860 67864 67870 67876 67878 67884 67888 67890 67896 67900 67906 67914 203614
(1)此消毒液可吸收空气中的CO2生成NaHCO3而变质.写出化学反应方程式______.
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出.通过以下装置检验气体的成分可以判断消毒液是否变质.
限选试剂:98%浓硫酸、1%品红溶液、1.0mol?L-1 KI-淀粉溶液、1.0mol?L-1NaOH、澄清石灰水、饱和NaCl溶液
请完成下列实验方案.
| 所加试剂 | 预期现象和结论 |
| 试管A中加足量①______; 试管B中加1%品红溶液; 试管C中加②______. | 若A中溶液变蓝色,B中溶液不退色,C中溶液变浑浊.则消毒液部分变质; ③______则消毒液未变质; ④______则消毒液完全变质. |
①量取25.00mL消毒液放入锥形瓶中,加入过量的a mol?L-1Na2SO3溶液b mL;
②滴定分析.将c mol?L-1的酸性KMnO4溶液装入______(填酸式或碱式)滴定管中;KMnO4和剩余的Na2SO3发生反应.当溶液由无色变成浅红色,且保持半分钟内红色不退时,停止滴定,记录数据.重复滴定实验2次,平均消耗酸性KMnO4溶液v mL;
滴定过程中涉及的反应有:NaClO+Na2SO3=NaCl+Na2SO4;2KMnO4+5Na2SO3+3H2SO4=K2SO4+2MnSO4+5Na2SO4+3H2O.
③计算.消毒液中NaClO的浓度为______mol?L-1(用含a、b、c、v的代数式表示).


 -ONa溶液中:若c(OH-)分别为c1、c2、c3,则c3>c2>c1
-ONa溶液中:若c(OH-)分别为c1、c2、c3,则c3>c2>c1