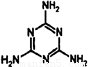
MnO2在酸性溶液中具有强氧化性,可被还原为Mn2+,它还对H2O2的分解具有良好的催化效果.某兴趣小组通过实验研究MnO2性质.
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是 .
A.把MnO2固体加入到FeSO4溶液中,再加入KSCN溶液,观察溶液是否变红
B.把MnO2固体加入到FeCl3溶液中,再加入KSCN溶液,观察溶液是否变红
C.把MnO2固体加入到Na2SO3溶液中,再加入BaCl2溶液,观察是否有白色沉淀生成
D.把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
(2)该小组为研究在不同酸碱性的溶液中MnO2的氧化能力,他们控制KI溶液的浓度和MnO2固体的质量相同,恒定实验温度在298K,设计如下对比实验:
①该小组从上述对比实验中,可以得出的结论是 .
②写出在酸性条件下MnO2氧化I-的离子方程式 .
(3)为了探究MnO2的催化效果,需要用30%的H2O2溶液(密度按1g/cm3)配制浓度为3%的H2O2溶液(密度按1g/cm3)100mL.配制过程中除了用到量筒、烧杯、100mL容量瓶外,还需用到的玻璃仪器名称是 ,需用量筒量取 mL30%的H2O2溶液.MnO2催化H2O2分解的化学方程式为 ,反应结束后将液体与MnO2分离的实验操作名称叫 .
(4)实验室用MnO2制取氯气的化学方程式为 .
0 67668 67676 67682 67686 67692 67694 67698 67704 67706 67712 67718 67722 67724 67728 67734 67736 67742 67746 67748 67752 67754 67758 67760 67762 67763 67764 67766 67767 67768 67770 67772 67776 67778 67782 67784 67788 67794 67796 67802 67806 67808 67812 67818 67824 67826 67832 67836 67838 67844 67848 67854 67862 203614
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是 .
A.把MnO2固体加入到FeSO4溶液中,再加入KSCN溶液,观察溶液是否变红
B.把MnO2固体加入到FeCl3溶液中,再加入KSCN溶液,观察溶液是否变红
C.把MnO2固体加入到Na2SO3溶液中,再加入BaCl2溶液,观察是否有白色沉淀生成
D.把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
(2)该小组为研究在不同酸碱性的溶液中MnO2的氧化能力,他们控制KI溶液的浓度和MnO2固体的质量相同,恒定实验温度在298K,设计如下对比实验:
| 实验 | 外加试剂 | 现象 |
| A | 1滴0.2mol/LNaOH溶液 | 不变色 |
| B | 1滴水 | 缓慢变浅棕褐色 |
| C | 1滴0.1mol/L硫酸 | 迅速变棕褐色 |
②写出在酸性条件下MnO2氧化I-的离子方程式 .
(3)为了探究MnO2的催化效果,需要用30%的H2O2溶液(密度按1g/cm3)配制浓度为3%的H2O2溶液(密度按1g/cm3)100mL.配制过程中除了用到量筒、烧杯、100mL容量瓶外,还需用到的玻璃仪器名称是 ,需用量筒量取 mL30%的H2O2溶液.MnO2催化H2O2分解的化学方程式为 ,反应结束后将液体与MnO2分离的实验操作名称叫 .
(4)实验室用MnO2制取氯气的化学方程式为 .
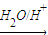 R-CH2CHO+R′OH,烃基烯基醚A的相对分子质量(M r)为176,分子中碳氢原子数目比为3:4.与A相关的反应如下
R-CH2CHO+R′OH,烃基烯基醚A的相对分子质量(M r)为176,分子中碳氢原子数目比为3:4.与A相关的反应如下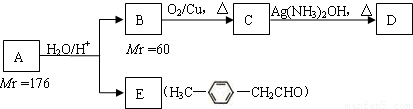
 H2C=CH2
H2C=CH2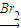 H2
H2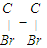 H2.
H2.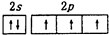
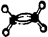 的球棍模型:
的球棍模型: