硫酸亚铁铵的化学式为(NH4)2Fe(SO4)2?6H2O,商品名为摩尔盐.硫酸亚铁可与硫酸铵生成硫酸亚铁铵,一般硫酸亚铁盐在空气中易被氧化,而形成摩尔盐后就比较稳定了.三种盐的溶解度(单位为g/100g水)如下表
实验室欲制备硫酸亚铁铵晶体,设计了如下方案.
(1)完成实验步骤中的填空:
①称取4g铁屑,放入小烧杯,加入15mL10%Na2CO3溶液,小火加热10min以除去______,倒掉溶液,用蒸馏水把铁冲洗干净,干燥,备用;
②将处理好的铁屑放入小烧杯,加入15mL 3mol/L H2SO4溶液,水浴加热至不再有气体生成为止,趁热过滤去剩余铁屑,并用少量热水洗涤烧杯及滤纸,并将滤液和洗涤液一起转移到蒸发皿中,则蒸发皿中溶液的溶质为______(填名称,不考虑水解),其物质的量约为______mol;
③加入______g硫酸铵到蒸发皿中,缓缓加热、浓缩至表面出现结晶膜为止、冷却,得硫酸亚铁铵晶体.
(2)回答下列问题:
①硫酸亚铁溶液在空气中易被氧化变质,操作时应注意:a______;b______;
②加热、浓缩溶液时,不浓缩至干的理由是______;
③硫酸亚铁和硫酸铵的混合溶液加热浓缩就能得到硫酸亚铁铵晶体,其原因是______;
④称取两份质量均为1.96g的该硫酸亚铁铵,制成溶液.用未知浓度的KMnO4酸性溶液进行滴定.
Ⅰ) 滴定时,将KMnO4酸性溶液装在______(酸式或碱式)滴定管,操作时用______手拿锥形瓶;
Ⅱ) 已知MnO4-被还原为Mn2+,试写出该滴定过程中的离子方程式:______;
Ⅲ) 判断该反应到达滴定终点的现象为______;
Ⅳ) 假设到达滴定终点时,用去V mL KMnO4酸性溶液,则该KMnO4酸性溶液的浓度为______mol/L.
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 70 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4?7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| (NH4)2Fe(SO4)2?6H2O | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
(1)完成实验步骤中的填空:
①称取4g铁屑,放入小烧杯,加入15mL10%Na2CO3溶液,小火加热10min以除去______,倒掉溶液,用蒸馏水把铁冲洗干净,干燥,备用;
②将处理好的铁屑放入小烧杯,加入15mL 3mol/L H2SO4溶液,水浴加热至不再有气体生成为止,趁热过滤去剩余铁屑,并用少量热水洗涤烧杯及滤纸,并将滤液和洗涤液一起转移到蒸发皿中,则蒸发皿中溶液的溶质为______(填名称,不考虑水解),其物质的量约为______mol;
③加入______g硫酸铵到蒸发皿中,缓缓加热、浓缩至表面出现结晶膜为止、冷却,得硫酸亚铁铵晶体.
(2)回答下列问题:
①硫酸亚铁溶液在空气中易被氧化变质,操作时应注意:a______;b______;
②加热、浓缩溶液时,不浓缩至干的理由是______;
③硫酸亚铁和硫酸铵的混合溶液加热浓缩就能得到硫酸亚铁铵晶体,其原因是______;
④称取两份质量均为1.96g的该硫酸亚铁铵,制成溶液.用未知浓度的KMnO4酸性溶液进行滴定.
Ⅰ) 滴定时,将KMnO4酸性溶液装在______(酸式或碱式)滴定管,操作时用______手拿锥形瓶;
Ⅱ) 已知MnO4-被还原为Mn2+,试写出该滴定过程中的离子方程式:______;
Ⅲ) 判断该反应到达滴定终点的现象为______;
Ⅳ) 假设到达滴定终点时,用去V mL KMnO4酸性溶液,则该KMnO4酸性溶液的浓度为______mol/L.
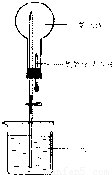
以下是某实验小组用CO2和NaOH溶液做喷泉实验的装置和测得的一组数据
已知:烧瓶最大容量为250mL,每次实验充分摇动烧瓶,只有NaOH浓度不同,其它条件和操作方式相同.结合喷泉实验原理及你所学的知识,判断下列说法中不正确的是______
A.CO2在水中的溶解度小,不宜用水直接吸收CO2来做喷泉实验
B.在一定的浓度范围内氢氧化钠溶液的浓度越大越易形成喷泉
C.NaOH浓度为1.6mol/L时,CO2还没有全部分被吸收
D.当氢氧化钠溶液的物质的量浓度为1.0mol/L时所得溶液不可能有氢氧化钠,烧瓶也没有充满.
| NaOH浓度(mol/L) | 0.4 | 0.5 | 0.8 | 1.0 | 1.4 | 1.6 | 1.8 | |
| 现象 | 不能 形成 | 一段 液柱 | 形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 |
| 时间 | 6min | 1min | 35s | 10s | 6s | 6s | ||
| 烧瓶中水的体积(mL) | 7 | 41 | 71 | 125 | 240 | 240 |
A.CO2在水中的溶解度小,不宜用水直接吸收CO2来做喷泉实验
B.在一定的浓度范围内氢氧化钠溶液的浓度越大越易形成喷泉
C.NaOH浓度为1.6mol/L时,CO2还没有全部分被吸收
D.当氢氧化钠溶液的物质的量浓度为1.0mol/L时所得溶液不可能有氢氧化钠,烧瓶也没有充满.

问题提出:小王同学有次实验时把SO2通入装有BaCl2、FeCl3的混合溶液的试管中,出现了白色浑浊物.
假设、验证:
请把上表填充完全.
(4)写出SO2通入BaCl2、FeCl3的混合溶液生成沉淀相关的离子方程式.______.
假设、验证:
| 假设 | 实验验证方法及现象 | |
| 假设1 | 白色浑浊物是BaSO3. | (1)______ |
假设2 | (2)白色浑浊物是BaSO4,主要 原因是______ . | 反应开始前,先向制取SO2的装置中通入纯净的CO2,再把产生的SO2通入BaCl2溶液中,不出现浑浊.滴加FeCl3溶液后出现浑浊 (3)通入纯净的CO2的目的______ |
(4)写出SO2通入BaCl2、FeCl3的混合溶液生成沉淀相关的离子方程式.______.
研制和开发不含碳并可工业生产的清洁能源,一直是科学家不懈追求的目标,目前液氨被人们视为一种潜在的清洁燃料.液氨燃烧的化学反应方程式为:4NH3+3O2→2N2+6H2O.和氢燃料相比有关数据见下表,据此判断正确的是( )
①以氨和氢为燃料时,可以减缓温室效应
②氨泄漏到空气中比氢气更易发生爆炸
③等质量的氨和氢分别燃烧,氢放出的热量少
④氮的液化比氢容易得多.
A.①③
B.②③
C.①④
D.②④
0 67634 67642 67648 67652 67658 67660 67664 67670 67672 67678 67684 67688 67690 67694 67700 67702 67708 67712 67714 67718 67720 67724 67726 67728 67729 67730 67732 67733 67734 67736 67738 67742 67744 67748 67750 67754 67760 67762 67768 67772 67774 67778 67784 67790 67792 67798 67802 67804 67810 67814 67820 67828 203614
| 燃料 | 沸点(℃) | 燃烧热(kJ/mol) | 相对分子质量 | 液态密度(g/cm3) |
| 氢 | -252.6 | 238.40 | 2.02 | 0.07 |
| 氨 | -33.50 | 317.10 | 17.03 | 0.61 |
②氨泄漏到空气中比氢气更易发生爆炸
③等质量的氨和氢分别燃烧,氢放出的热量少
④氮的液化比氢容易得多.
A.①③
B.②③
C.①④
D.②④