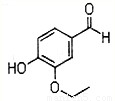
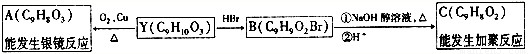25时,部分弱酸的电离平衡常数如下表:
下列有关说法正确的是( )
A.等物质的量浓度溶液的pH关系为pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B.a mol?L-1HCN溶液与b mol?L-1NaOH溶液等体积混合后,所得溶液中:C(Na+)>c(CN-),则a一定小于b
C.往冰醋酸中逐滴加水,溶液的导电性先增大后减小
D.NaHCO3和Na2CO3的混合液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
A.等物质的量浓度溶液的pH关系为pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B.a mol?L-1HCN溶液与b mol?L-1NaOH溶液等体积混合后,所得溶液中:C(Na+)>c(CN-),则a一定小于b
C.往冰醋酸中逐滴加水,溶液的导电性先增大后减小
D.NaHCO3和Na2CO3的混合液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)
X、Y、Z、M是由短周期元素组成的化合物;X、Y、Z均含有钠元素,且Y、Z均含有三种元素;Z的溶液显碱性.请回答下列问题:
(1)X为淡黄色粉末,可作潜水艇的供氧剂,则X为______.X中除钠元素外,其它元素的原子结构示意图为______.
(2)Y、Z、M有关实验如下表:
①Y中阴离子的结构如图所示,可以看成是SO42-中的一个O原子被S原子所替代,请写出Y与稀H2SO4反应的离子方程式:______.

②写出含0.1mol Z的溶液与20mL 2.5mol?L-1M的溶液反应的化学方程式:______.
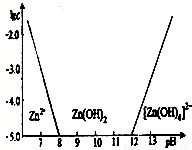
(3)如图所示,横坐标表示常温下溶液的pH,纵坐标可表示Zn2+、[Zn(OH)4]2-浓度的对数值(lgc).请回答下列问题:
①ZnCl2溶液呈酸性的原因是______
(1)X为淡黄色粉末,可作潜水艇的供氧剂,则X为______.X中除钠元素外,其它元素的原子结构示意图为______.
(2)Y、Z、M有关实验如下表:
| 实验 | 主要实验步骤及实验现象 |
| 1 | 向Y溶液中加入稀H2SO4,产生淡黄色沉淀和无色有刺激性气味的气体,该气体能使品红溶液退色. |
| 2 | 向M溶液中连续滴加Z溶液,初有白色沉淀,后沉淀溶解. |
| 3 | 向M稀溶液中滴加硝酸酸化的硝酸银溶液,产生白色沉淀. |

②写出含0.1mol Z的溶液与20mL 2.5mol?L-1M的溶液反应的化学方程式:______.
(3)如图所示,横坐标表示常温下溶液的pH,纵坐标可表示Zn2+、[Zn(OH)4]2-浓度的对数值(lgc).请回答下列问题:

①ZnCl2溶液呈酸性的原因是______
随着环保意识增强,清洁能源越来越受到人们关注.
(1)甲烷是一种理想的洁净燃料.已知:
CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-802.3kJ?mol-1
H2O(1)=H2O(g)△H=+44.0kJ?mol-1
则4.8g甲烷气体完全燃烧生成液态水,放出热量为______.
(2)利用甲烷与水反应制备氢气,因原料廉价,具有推广价值.
该反应为CH4(g)+H2O(g)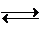 CO(g)+3H2(g)△H=+206.1kJ?mol-1.
CO(g)+3H2(g)△H=+206.1kJ?mol-1.
①若800℃时,反应的化学平衡常数K=l.0,某时刻测得该温度下密闭容器中各物质的物质的量浓度如下表.
则此时正、逆反应速率的关系是______.(填下列相关选项的字母符号)
A.v(正)>v(逆) B.v(正)<v(逆)C.v(正)=v(逆)D.无法判断
②为了探究温度、压强对上述化学反应速率的影响,张山同学设计了以下三组对比实验(温度为360℃或480℃、压强为101kPa或303kPa,其余实验条件见下表).
表中t=______,P=______;
设计实验2、3的目的是______;
实验l、2、3中反应的化学平衡常数的大小关系是______(用K1、K2、K3表示).
(3)利用催化剂,通过两步反应可将水分解制得氢气,若第一步反应为:MnFe2O4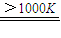 MnFe2O4-x+
MnFe2O4-x+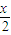 □↑,则框内物质为______;
□↑,则框内物质为______;
第二步反应的化学方程式为______(可不写反应条件).
(1)甲烷是一种理想的洁净燃料.已知:
CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-802.3kJ?mol-1
H2O(1)=H2O(g)△H=+44.0kJ?mol-1
则4.8g甲烷气体完全燃烧生成液态水,放出热量为______.
(2)利用甲烷与水反应制备氢气,因原料廉价,具有推广价值.
该反应为CH4(g)+H2O(g)
①若800℃时,反应的化学平衡常数K=l.0,某时刻测得该温度下密闭容器中各物质的物质的量浓度如下表.
| CH4 | H2O | CO | H2 |
| 3.0mol?L-1 | 8.5mol?L-1 | 2.0mol?L-1 | 2.0mol?L-1 |
A.v(正)>v(逆) B.v(正)<v(逆)C.v(正)=v(逆)D.无法判断
②为了探究温度、压强对上述化学反应速率的影响,张山同学设计了以下三组对比实验(温度为360℃或480℃、压强为101kPa或303kPa,其余实验条件见下表).
| 实验序号 | 温度/℃ | 压强/kPa | CH4初始浓度/mol?L-1 | H2O初始浓度/mol?L-1 | K |
| 1 | 360 | P | 2.00 | 6.80 | K1 |
| 2 | t | 101 | 2.00 | 6.80 | K2 |
| 3 | 360 | 101 | 2.00 | 6.80 | K3 |
设计实验2、3的目的是______;
实验l、2、3中反应的化学平衡常数的大小关系是______(用K1、K2、K3表示).
(3)利用催化剂,通过两步反应可将水分解制得氢气,若第一步反应为:MnFe2O4
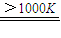 MnFe2O4-x+
MnFe2O4-x+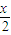 □↑,则框内物质为______;
□↑,则框内物质为______;第二步反应的化学方程式为______(可不写反应条件).
铜及其化合物在生产和生活实际中应用广泛.
Ⅰ.某学习小组对粗铜提纯(电解精炼)后的阳极泥(主要成分为银、金)进行如下实验.
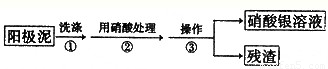
(1)操作③所需的仪器有:烧杯、______.
(2)为了回收金,他们查阅了有关资料如表:
从资料中可知,常温下金很难与硝酸反应,但却可溶于王水(浓硝酸与浓盐酸体积比为1:3的混合物).请你运用化学平衡移动原理,简要说明金能溶于王水的原因:______.
Ⅱ.学习小组对无水硫酸铜分解的产物进行实验探究.
[提出问题]碳酸钙受热分解生成CaO和CO2,那么无水硫酸铜受热分解也只生成CuO和SO3吗?
[设计实验]按如图装置进行试验.
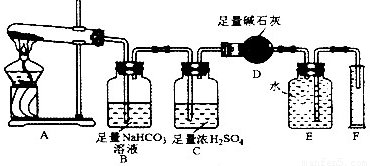
[实验过程]
a.准确称取无水硫酸铜2.40g于装置A试管中加热,直至固体全部变为黑色,经验证该黑色粉末为CuO
b.实验中,观察到装置E中的水部分被排入量筒中;实验结束后,测得量筒中水的体积为112mL(已折算成标准状态下气体的体积),并测得干燥管D的质量增加了1.32g.
(3)装置C的作用______.
(4)根据装置E、F中现象,推测还有气体______(填分子式)生成;实验生成的SO3为______ mol.
(5)装置A中反应的化学方程式为______ 3CuO+2SO2↑+SO3↑+O2↑
Ⅰ.某学习小组对粗铜提纯(电解精炼)后的阳极泥(主要成分为银、金)进行如下实验.

(1)操作③所需的仪器有:烧杯、______.
(2)为了回收金,他们查阅了有关资料如表:
| 编号 | 常温下反应 | 化学平衡常数 |
| 反应1 | Au+6HNO3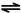 Au(NO3)3+3NO2↑+3H2O Au(NO3)3+3NO2↑+3H2O | <10-5 |
| 反应2 | Au3++Cl- 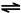 [AuCl4]- [AuCl4]- | >105 |
Ⅱ.学习小组对无水硫酸铜分解的产物进行实验探究.
[提出问题]碳酸钙受热分解生成CaO和CO2,那么无水硫酸铜受热分解也只生成CuO和SO3吗?
[设计实验]按如图装置进行试验.

[实验过程]
a.准确称取无水硫酸铜2.40g于装置A试管中加热,直至固体全部变为黑色,经验证该黑色粉末为CuO
b.实验中,观察到装置E中的水部分被排入量筒中;实验结束后,测得量筒中水的体积为112mL(已折算成标准状态下气体的体积),并测得干燥管D的质量增加了1.32g.
(3)装置C的作用______.
(4)根据装置E、F中现象,推测还有气体______(填分子式)生成;实验生成的SO3为______ mol.
(5)装置A中反应的化学方程式为______ 3CuO+2SO2↑+SO3↑+O2↑
[化学-物质结构与性质]
W、X、Y、Z 4种元素原子序数依次减小.W的原子序数为24;X原子p轨道共有11个电子;Y是第三周期主族元素,其部分电离能(I)如下表;Z原子价电子排布式为nsnnpn.请回答下列问题:
(1)W基态原子的电子排步式为______.
(2)电负性:X______Y(填“>”、“=”或“<”).
(3)R是与X同主族的短周期元素.R的氢化物沸点比X的氢化物更高,原因是:______.
(4)氨为常见化工原料,氨分子中N原子采用______杂化,该分子的空间构型为______,分子中N、H原子之间形成______(填“σ”或“π”)键;
已知W3+能与氨分子形成配离子[W(NH3)6]3+,该配离子中存在的化学键有______.(填标号)
A.金属键 B.离子键 C.共价键 D.配位键.
0 67623 67631 67637 67641 67647 67649 67653 67659 67661 67667 67673 67677 67679 67683 67689 67691 67697 67701 67703 67707 67709 67713 67715 67717 67718 67719 67721 67722 67723 67725 67727 67731 67733 67737 67739 67743 67749 67751 67757 67761 67763 67767 67773 67779 67781 67787 67791 67793 67799 67803 67809 67817 203614
W、X、Y、Z 4种元素原子序数依次减小.W的原子序数为24;X原子p轨道共有11个电子;Y是第三周期主族元素,其部分电离能(I)如下表;Z原子价电子排布式为nsnnpn.请回答下列问题:
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 | I5 |
| Y | 584 | 1823 | 2751 | 11584 | 14837 |
(2)电负性:X______Y(填“>”、“=”或“<”).
(3)R是与X同主族的短周期元素.R的氢化物沸点比X的氢化物更高,原因是:______.
(4)氨为常见化工原料,氨分子中N原子采用______杂化,该分子的空间构型为______,分子中N、H原子之间形成______(填“σ”或“π”)键;
已知W3+能与氨分子形成配离子[W(NH3)6]3+,该配离子中存在的化学键有______.(填标号)
A.金属键 B.离子键 C.共价键 D.配位键.