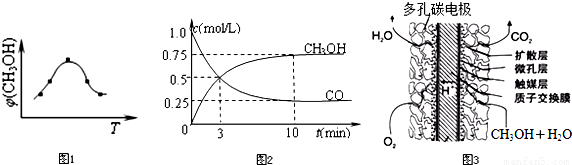
下列有关化学反应现象或化学原理的解释正确的是( )
A.A
B.B
C.C
D.D
| 选项 | 现象或反应 | 原理解释 |
| A | KI淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪去 | SO2具有漂白性 |
| B | 合成氨反应需在高温条件下进行 | 该反应为吸热反应 |
| C | 蒸馏时,温度计的球泡应靠近蒸馏烧瓶支管口处 | 此位置指示的是被蒸馏物质的沸点 |
| D | 2CO=2C+O2在任何条件下均不能自发进行 | 该反应△H>0,△S<0 |
A.A
B.B
C.C
D.D
利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理.
(1)染料工业排放的废水中含有大量有毒的NO2¯,可以在碱性条件下加入铝粉除去(加热处理后的废水,会产生能使湿润的红色石蕊试纸变蓝的气体).除去NO2¯离子的离子方程式为______.
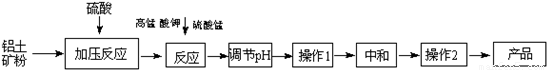
(2)某工厂对制革工业污泥中Cr3+回收与再利用工艺如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe2+、Fe3+、Al3+、Ca2+、Mg2+):
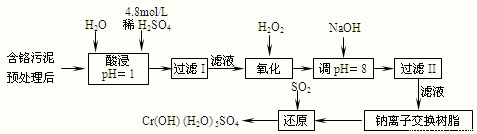
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见表:
①实验室用18.4mol/L的浓硫酸配制250mL 4.8mol/L的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需______.
②酸浸时,为了提高浸取率可采取的措施是______(答2点).
③加入H2O2的作用是______.
④钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的杂质离子是______(选填:Fe3+、Al3+、Ca2+、Mg2+).
(3)印刷电路铜板腐蚀剂常用FeCl3.腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol/L,请参照上表给出的数据和提供的试剂(可能用到的试剂:Cl2、浓H2SO4、NaOH溶液、CuO、Cu),简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤①______;②______;③过滤.
0 67594 67602 67608 67612 67618 67620 67624 67630 67632 67638 67644 67648 67650 67654 67660 67662 67668 67672 67674 67678 67680 67684 67686 67688 67689 67690 67692 67693 67694 67696 67698 67702 67704 67708 67710 67714 67720 67722 67728 67732 67734 67738 67744 67750 67752 67758 67762 67764 67770 67774 67780 67788 203614
(1)染料工业排放的废水中含有大量有毒的NO2¯,可以在碱性条件下加入铝粉除去(加热处理后的废水,会产生能使湿润的红色石蕊试纸变蓝的气体).除去NO2¯离子的离子方程式为______.
(2)某工厂对制革工业污泥中Cr3+回收与再利用工艺如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe2+、Fe3+、Al3+、Ca2+、Mg2+):

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | -- | -- | 4.7 | -- |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9 (>9溶解) |
②酸浸时,为了提高浸取率可采取的措施是______(答2点).
③加入H2O2的作用是______.
④钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的杂质离子是______(选填:Fe3+、Al3+、Ca2+、Mg2+).
(3)印刷电路铜板腐蚀剂常用FeCl3.腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol/L,请参照上表给出的数据和提供的试剂(可能用到的试剂:Cl2、浓H2SO4、NaOH溶液、CuO、Cu),简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤①______;②______;③过滤.