(1)一定温度下,在恒容密闭容器中NO2与O2反应如下:4NO2(g)+O2(g)?2N2O5(g);若已知K350℃<K300℃,则该反应是______反应(填“吸热”或“放热”).反应达平衡后,若再通入一定量NO2,则平衡常数K将______,NO2的转化率______(填“增大”、“减小”或“不变”)
(2)若初始时在恒容密闭容器中加入N2O5,下表为N2O5分解反应在一定温度下不同时间测得N2O5浓度的部分实验数据:
①写出该反应的平衡常数表达式:K=______.
②1000s内N2O5的分解速率为______.
③若每有1molN2O5分解,放出或吸收QkJ的热量,写出该分解反应的热化学方程式______.
0 67449 67457 67463 67467 67473 67475 67479 67485 67487 67493 67499 67503 67505 67509 67515 67517 67523 67527 67529 67533 67535 67539 67541 67543 67544 67545 67547 67548 67549 67551 67553 67557 67559 67563 67565 67569 67575 67577 67583 67587 67589 67593 67599 67605 67607 67613 67617 67619 67625 67629 67635 67643 203614
(2)若初始时在恒容密闭容器中加入N2O5,下表为N2O5分解反应在一定温度下不同时间测得N2O5浓度的部分实验数据:
| t/s | 500 | 1000 | |
| c(N2O5)/mol?L-1 | 5.00 | 3.52 | 2.48 |
②1000s内N2O5的分解速率为______.
③若每有1molN2O5分解,放出或吸收QkJ的热量,写出该分解反应的热化学方程式______.

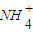 )>c(Na+ )>c(OH-)>c(H+)
)>c(Na+ )>c(OH-)>c(H+)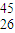 Fe原子,有关
Fe原子,有关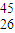 Fe的说法正确的是( )
Fe的说法正确的是( )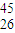 Fe与
Fe与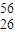 Fe互为同素异形体
Fe互为同素异形体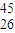 Fe的中子数是26
Fe的中子数是26
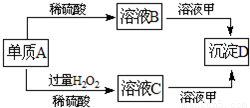
 (“→”表示一步完成)关系相互转化的是( )
(“→”表示一步完成)关系相互转化的是( )