科学家一直致力于“人工固氮”的新方法研究.最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂表面与水发生下列反应:
2N2(g)+6H2O(l) 4NH3 (g)+3O2(g)△H=a kJ?mol-1
4NH3 (g)+3O2(g)△H=a kJ?mol-1
上述反应NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
(1)此合成反应的a______0 (填“>”“<”或“=”)
(2)用水稀释0.1mol?L-1氨水,溶液中随着水量的增加而减小的是______(填字母标号)
A.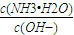 B.
B.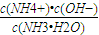 C.c(H+)?c(OH-) D.
C.c(H+)?c(OH-) D.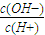
(3)氨可用于工业制硝酸,其主反应为:
4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H<0
若此反应起始的物质的量相同,则下列关系图正确的是______(填序号)
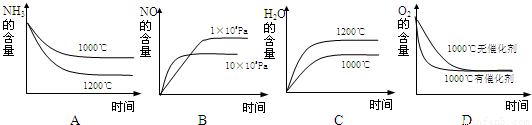
(4)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
①反应在第2min到第4min时,O2 的平均反应速率为______mol/
②反应在第2min到第4min时改变了条件,改变的条件可能是______.
③在第6min到第8min时,改变了反应的条件,该平衡向______移动(填“左”或“右”).
2N2(g)+6H2O(l)
 4NH3 (g)+3O2(g)△H=a kJ?mol-1
4NH3 (g)+3O2(g)△H=a kJ?mol-1上述反应NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
| 温度 T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
(2)用水稀释0.1mol?L-1氨水,溶液中随着水量的增加而减小的是______(填字母标号)
A.
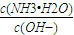 B.
B.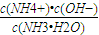 C.c(H+)?c(OH-) D.
C.c(H+)?c(OH-) D.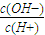
(3)氨可用于工业制硝酸,其主反应为:
4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H<0
若此反应起始的物质的量相同,则下列关系图正确的是______(填序号)

(4)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
| 时间/浓度 | c(NH3) (mol/L) | c(O2 ) (mol/L) | c(NO) (mol/L) |
| 起始 | 0.8000 | 1.600 | 0.000 |
| 第2min | 0.6000 | a | 0.2000 |
| 第4min | 0.3000 | 0.9750 | 0.5000 |
| 第6min | 0.3000 | 0.9750 | 0.5000 |
| 第8min | 0.7000 | 1.475 | 0.1000 |
②反应在第2min到第4min时改变了条件,改变的条件可能是______.
③在第6min到第8min时,改变了反应的条件,该平衡向______移动(填“左”或“右”).
高铁酸盐(K2FeO4、Na2FeO4)在能源、环保等方面有着广泛的用途.干法、湿法制备高铁酸盐的原理如下表所示.
 △
△
(1)干法制备K2FeO4的化学方程式为Fe2O3+3KNO3+4KOH═2K2FeO4+3KNO2+2H2O,该反应中氧化剂与还原剂的物质的量之比为______.
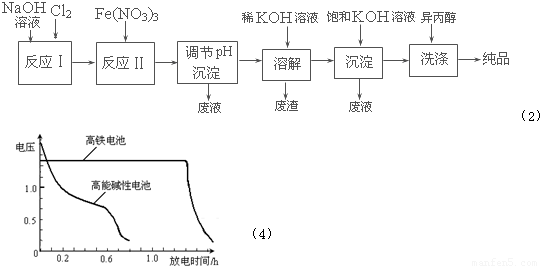
(2)工业上用湿法制备高铁酸钾(K2FeO4)的流程如下图所示:溶解
①反应I的化学方程式为______.
②反应II的离子方程式为______.
③加入饱和KOH溶液的目的是______.
(3)高铁酸钾在水中既能消毒杀菌,又能净水,是一种理想的水处理剂.它能消毒杀菌是因为______,它能净水的原因是
______.
(4)高铁电池是正在研制中的可充电干电池,右图为高铁电池和常用的高能碱性电池的放电曲线,由图可得出高铁电池的优点有:工作电压稳定,______.
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色K2FeO4和KNO2等产物 |
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色Na2FeO4溶液 |
 △
△(1)干法制备K2FeO4的化学方程式为Fe2O3+3KNO3+4KOH═2K2FeO4+3KNO2+2H2O,该反应中氧化剂与还原剂的物质的量之比为______.
(2)工业上用湿法制备高铁酸钾(K2FeO4)的流程如下图所示:溶解
①反应I的化学方程式为______.
②反应II的离子方程式为______.
③加入饱和KOH溶液的目的是______.
(3)高铁酸钾在水中既能消毒杀菌,又能净水,是一种理想的水处理剂.它能消毒杀菌是因为______,它能净水的原因是
______.
(4)高铁电池是正在研制中的可充电干电池,右图为高铁电池和常用的高能碱性电池的放电曲线,由图可得出高铁电池的优点有:工作电压稳定,______.
某化学兴趣小组在探究次氯酸钠溶液的性质时发现:往过量FeSO4溶液中滴入几滴NaClO溶液,并加入适量硫酸,溶液立即变黄.请你协助他们完成该反应还原产物的探究.
(1)甲同学推测该反应的还原产物为Cl2;乙同学推测该反应的还原产物为______.
(2)你认为甲同学的推测是否正确?______(填“正确”或“不正确”).请用简要的文字或离子方程式说明理由______.
根据乙同学的推测,上述反应的离子方程式为______.
(3)请你设计一个实验方案,验证乙同学的推测(还原产物)是否正确.要求在答题卡上按下表格式写出实验步骤、预期现象和结论:
0 67373 67381 67387 67391 67397 67399 67403 67409 67411 67417 67423 67427 67429 67433 67439 67441 67447 67451 67453 67457 67459 67463 67465 67467 67468 67469 67471 67472 67473 67475 67477 67481 67483 67487 67489 67493 67499 67501 67507 67511 67513 67517 67523 67529 67531 67537 67541 67543 67549 67553 67559 67567 203614
(1)甲同学推测该反应的还原产物为Cl2;乙同学推测该反应的还原产物为______.
(2)你认为甲同学的推测是否正确?______(填“正确”或“不正确”).请用简要的文字或离子方程式说明理由______.
根据乙同学的推测,上述反应的离子方程式为______.
(3)请你设计一个实验方案,验证乙同学的推测(还原产物)是否正确.要求在答题卡上按下表格式写出实验步骤、预期现象和结论:
| 实验操作 | 预期现象和结论 |
| 步骤1: | ______ |
| 步骤2: | ______ |
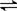 Fe(SCN)2+ (aq);已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如下图所示,则下列说法正确的是( )
Fe(SCN)2+ (aq);已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如下图所示,则下列说法正确的是( )

 有机物互为同分异构体
有机物互为同分异构体