请仔细观察两种电池的构造示意图,回答下列问题:
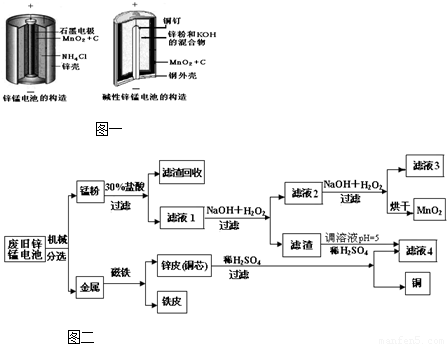
(1)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应式: .
(2)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大.试从影响反应速率的因素分析其原因是 .
(3)某工厂回收废旧锌锰电池,其工艺流程如图二:
已知:生成氢氧化物的pH如下表:
①经测定,“锰粉”中除含少量铁盐和亚铁盐外,主要成分应是MnO2、Zn(OH)2 .②第一次加入H2O2后,调节pH=8.0.目的是 ③试列举滤液4的应用实例 .

(1)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应式: .
(2)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大.试从影响反应速率的因素分析其原因是 .
(3)某工厂回收废旧锌锰电池,其工艺流程如图二:
已知:生成氢氧化物的pH如下表:
| 物质 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 5.7 | 8.3 |
| 完全沉淀pH | 3.7 | 9.6 | 8.0 | 9.8 |
向一体积不变的密闭容器中加入2mol A、0.6molC和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如附图一所示.附图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件.已知t3-t4阶段为使用催化剂;图一中t-t1阶段c(B)未画出.

(1)若t1=15min,则t-t1阶段以C浓度变化表示的反应速率为v(C)= .
(2)t4-t5阶段改变的条件为 ,B的起始物质的量为 .各阶段平衡时对应的平衡常数如下表所示:
K1、K2、K3、K4、K5之间的关系为 求出K1(写过程).
(3)t5-t6阶段保持容器内温度不变,若A的物质的量共变化了0.01mol,而此过程中容器与外界的热交换总量为akJ,写出此温度下该反应的热化学方程式 .
(4)在相同条件下,若起始时容器中加入a molA、bmolB和cmolC,要达到t1时刻同样的平衡,a、b、c要满足的条件为 .
0 67323 67331 67337 67341 67347 67349 67353 67359 67361 67367 67373 67377 67379 67383 67389 67391 67397 67401 67403 67407 67409 67413 67415 67417 67418 67419 67421 67422 67423 67425 67427 67431 67433 67437 67439 67443 67449 67451 67457 67461 67463 67467 67473 67479 67481 67487 67491 67493 67499 67503 67509 67517 203614

(1)若t1=15min,则t-t1阶段以C浓度变化表示的反应速率为v(C)= .
(2)t4-t5阶段改变的条件为 ,B的起始物质的量为 .各阶段平衡时对应的平衡常数如下表所示:
| t1-t2 | t2-t3 | t3-t4 | t4-t5 | t5-t6 |
| K1 | K2 | K3 | K4 | K5 |
(3)t5-t6阶段保持容器内温度不变,若A的物质的量共变化了0.01mol,而此过程中容器与外界的热交换总量为akJ,写出此温度下该反应的热化学方程式 .
(4)在相同条件下,若起始时容器中加入a molA、bmolB和cmolC,要达到t1时刻同样的平衡,a、b、c要满足的条件为 .





 2H++S2-
2H++S2-