已知a、e、I为三种由短周期元素构成的10个电子的粒子,其结构特点如下:
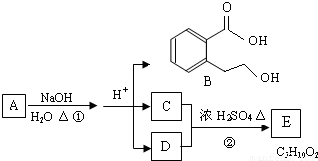
物质A由a、e 构成,B、C、D、K都是单质,各有关物质之间的相互反应转化关系如下图所示,反应①-⑤都是用于工业生产的反应,⑥、⑦反应中个别产物在图中略去.请填写下列空白:
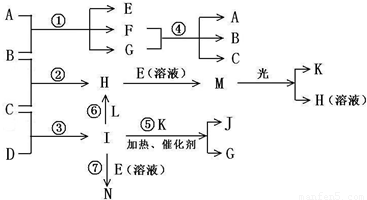
(1)写出下列物质的化学式:B______,J______.
(2)写出下列反应的离子反应方程式:H+E(溶液)→M______,F+G→A+B+C______ Cl2+H2+2OH-
| 粒子代码 | a | e | I |
| 原子核数 | 单核 | 两核 | 四核 |
| 粒子的电荷数 | 一个单位正电荷 | 一个单位负电荷 |

(1)写出下列物质的化学式:B______,J______.
(2)写出下列反应的离子反应方程式:H+E(溶液)→M______,F+G→A+B+C______ Cl2+H2+2OH-
已知25℃时部分弱电解质的电离平衡常数数据如下表:
回答下列问题:
(1)物质的量浓度均为0.1mol?L-1的四种溶液:a.CH3COOH b.Na2CO3 c.NaClO d.NaHCO3;pH由小到大的排列顺序是 (用字母表示)
(2)常温下,0.1mol?L-1的CH3COOH溶液加稀释过程中,下列表达式的数据变大的是
A.c(H+)B.c(H+)/c(CH3COOH)
C.c(H+)?c(OH-)D.c(OH-)/c(H+)
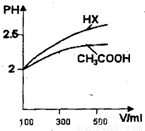
(3)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数 CH3COOH的电离平衡常数(填大于、小于或等于)理由是
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)= mol?L-1(填精确值),c(CH3COO-)/c(CH3COOH)= .
0 67316 67324 67330 67334 67340 67342 67346 67352 67354 67360 67366 67370 67372 67376 67382 67384 67390 67394 67396 67400 67402 67406 67408 67410 67411 67412 67414 67415 67416 67418 67420 67424 67426 67430 67432 67436 67442 67444 67450 67454 67456 67460 67466 67472 67474 67480 67484 67486 67492 67496 67502 67510 203614
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-4 |
(1)物质的量浓度均为0.1mol?L-1的四种溶液:a.CH3COOH b.Na2CO3 c.NaClO d.NaHCO3;pH由小到大的排列顺序是 (用字母表示)
(2)常温下,0.1mol?L-1的CH3COOH溶液加稀释过程中,下列表达式的数据变大的是
A.c(H+)B.c(H+)/c(CH3COOH)
C.c(H+)?c(OH-)D.c(OH-)/c(H+)
(3)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数 CH3COOH的电离平衡常数(填大于、小于或等于)理由是
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)= mol?L-1(填精确值),c(CH3COO-)/c(CH3COOH)= .

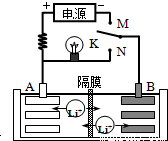
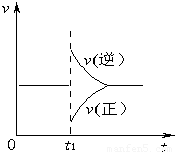
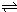 2SO3(g)△H<0在一定条件下达到平衡状态,时间为t1时改变条件.化学反应速率与反应时间关系如图.下列说法中正确的是( )
2SO3(g)△H<0在一定条件下达到平衡状态,时间为t1时改变条件.化学反应速率与反应时间关系如图.下列说法中正确的是( )