近期因“召回门”而闹的沸沸扬扬的丰田Prius属第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态.
(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,每生成1mol水蒸气放热569.1kJ.则该反应的热化学方程式为______.
(2)混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解液.镍氢电池充放电原理示意如图,其总反应式是:H2+2NiOOH 2Ni(OH)2.根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH将______(填“增大”、“不变”或“减小”),该电极的电极反应式为______.
2Ni(OH)2.根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH将______(填“增大”、“不变”或“减小”),该电极的电极反应式为______.
(3)汽车尾气中的一氧化碳是大气污染物,可通过如下反应降低其浓度:CO(g)+ O2(g)?CO2(g).
O2(g)?CO2(g).
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如下表所示.请填写表中的空格.
②相同温度下,某汽车尾气中CO、CO2的浓度分别为1.0×10-5mol?L-1和1.0×10-4mol?L-1.若在汽车的排气管上增加一个补燃器,不断补充O2并使其浓度保持为1.0×10-4mol?L-1,则最终尾气中CO的浓度为______mol?L-1.

(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,每生成1mol水蒸气放热569.1kJ.则该反应的热化学方程式为______.
(2)混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解液.镍氢电池充放电原理示意如图,其总反应式是:H2+2NiOOH
 2Ni(OH)2.根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH将______(填“增大”、“不变”或“减小”),该电极的电极反应式为______.
2Ni(OH)2.根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH将______(填“增大”、“不变”或“减小”),该电极的电极反应式为______.(3)汽车尾气中的一氧化碳是大气污染物,可通过如下反应降低其浓度:CO(g)+
 O2(g)?CO2(g).
O2(g)?CO2(g).①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如下表所示.请填写表中的空格.
| 容器编号 | c(CO)/mo1?L-1 | c (02)/mol?L-1 | c (C02)/mol?L-1 | v(正)和v (逆)比较 |
| I | 2.0×10-4 | 4.0×10-4 | 4.0×10-2 | v(正)=v(逆) |
| Ⅱ | 3.0×10-4 | 4.0×10-4 | 5.0×10-2 | ______ |

[化学选修2:化学与技术]工业上为了使原料和能量得到充分的利用,常常采用循环操作.
Ⅰ、利用热化学循环制氢能缓解能源矛盾.最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢.MnFe2O4的制备:
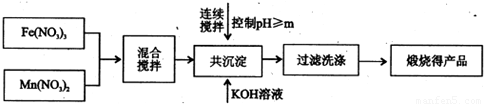
已知Fe3+、Mn2+沉淀的pH如表所示.
(1)此工艺中理论上投入原料Fe(NO3)3和Mn(NO3)2的物质的量之比应为______.
(2)控制pH的操作中m的值为______.
Ⅱ、用MnFe2O4热化学循环制取氢气:MnFe2O4(s)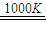 MnFe2O(4-x)(s)+
MnFe2O(4-x)(s)+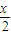 8O2(g);△H1=akJ/mol,
8O2(g);△H1=akJ/mol,
MnFe2O(4-x)(s)+xH2O(l)═MnFe2O4(s)+xH2(g);△H2=bkJ/mol,
(3)由上可知,H2燃烧的热化学方程式是______.
(4)该热化学循环制取氢气的优点是______(填字母编号).
A.过程简单、无污染 B.物料可循环使用 C.氧气和氢气在不同步骤生成,安全且易分离
Ⅲ、工业上可用H2、HCl通过如图的循环流程制取太阳能材料高纯硅.
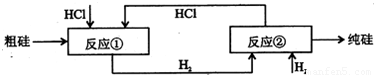
反应①Si(粗)+3HCl(g)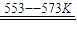 SiHCI3(l)+H2(g)
SiHCI3(l)+H2(g)
反应②:SiHCl3(l)+H2(g)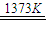 Si(纯)+3HCl(g)
Si(纯)+3HCl(g)
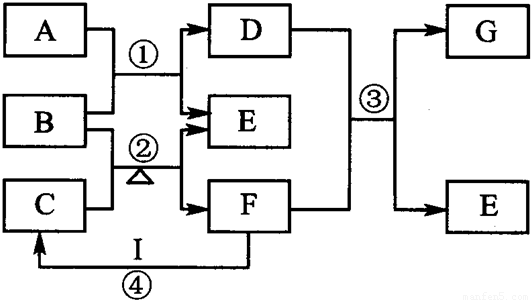
(5)上图中,假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率和反应②中H2的利用率均为75%.则在下一轮次的生产中,需补充投入HCl和H2的体积比是______.
0 67266 67274 67280 67284 67290 67292 67296 67302 67304 67310 67316 67320 67322 67326 67332 67334 67340 67344 67346 67350 67352 67356 67358 67360 67361 67362 67364 67365 67366 67368 67370 67374 67376 67380 67382 67386 67392 67394 67400 67404 67406 67410 67416 67422 67424 67430 67434 67436 67442 67446 67452 67460 203614
Ⅰ、利用热化学循环制氢能缓解能源矛盾.最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢.MnFe2O4的制备:

已知Fe3+、Mn2+沉淀的pH如表所示.
| 开始沉淀 | 完全沉淀 | |
| Fe3+ | 2.7 | 4.2 |
| Mn2+ | 8.3 | 10.4 |
(2)控制pH的操作中m的值为______.
Ⅱ、用MnFe2O4热化学循环制取氢气:MnFe2O4(s)
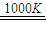 MnFe2O(4-x)(s)+
MnFe2O(4-x)(s)+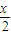 8O2(g);△H1=akJ/mol,
8O2(g);△H1=akJ/mol,MnFe2O(4-x)(s)+xH2O(l)═MnFe2O4(s)+xH2(g);△H2=bkJ/mol,
(3)由上可知,H2燃烧的热化学方程式是______.
(4)该热化学循环制取氢气的优点是______(填字母编号).
A.过程简单、无污染 B.物料可循环使用 C.氧气和氢气在不同步骤生成,安全且易分离
Ⅲ、工业上可用H2、HCl通过如图的循环流程制取太阳能材料高纯硅.

反应①Si(粗)+3HCl(g)
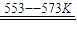 SiHCI3(l)+H2(g)
SiHCI3(l)+H2(g)反应②:SiHCl3(l)+H2(g)
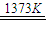 Si(纯)+3HCl(g)
Si(纯)+3HCl(g)(5)上图中,假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率和反应②中H2的利用率均为75%.则在下一轮次的生产中,需补充投入HCl和H2的体积比是______.
 2SO3(g).初始时两容器的温度、体积相同,一段时间后反应达到平衡,为使两容器中的SO2在平衡混合物中的物质的量分数相同,下列措施中可行的是( )
2SO3(g).初始时两容器的温度、体积相同,一段时间后反应达到平衡,为使两容器中的SO2在平衡混合物中的物质的量分数相同,下列措施中可行的是( )