柴达木盆地以青藏高原“聚宝盆”之誉蜚声海内外,它有富足得令人惊讶的盐矿资源.液体矿床以钾矿为主,伴生着镁、溴等多种矿产.某研究性学习小组拟取盐湖苦卤的浓缩液(富含K+、Mg2+、Br-、SO42-、Cl-等),来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程图1:

请根据以上流程,回答相关问题:
(1)操作①的名称:______;操作②名称是:______;
操作③的名称是:______;
操作④需要的玻璃仪器有:______.
(2)参照图2溶解度曲线,欲得到较纯的氯化钾晶体需用少量的______(选填:“热水”,“冷水”)洗涤固体______(选填“A”或“B”).
(3)同学甲提出一些新的方案,对上述操作②后无色溶液进行除杂提纯,其方案如下:
【有关资料】
【设计除杂过程】

(i)若在图3的操作⑤结束后发现溶液B略有浑浊,应采取的措施是______,
(ii)混合液A的主要成分是______.(填化学式)
【检验除杂效果】
(ⅲ)为检验Mg2+、SO42-是否除尽,通常分别取悬浊液A上层清液于两试管中.进行如下实验:
步骤一:检验Mg2+是否除尽.向其中一支试管中加入______溶液(填化学式),如果没有沉淀生成,则Mg2+已除尽.
步骤二:检验SO42-是否除尽.向另一支试管中加入某溶液,如果无有沉淀生成,则SO42-已除尽,效果最好的是______(填字母).
A.Na2 CO3 B.BaCl2 C.CaCl2
【获取纯净氯化钾】
(ⅳ)对溶液B加热并不断滴加l mol?L一1的盐酸溶液,同时用pH试纸检测溶液,直至pH=5时停止加盐酸,得到溶液C.该操作的目的是______.
(ⅴ)将溶液C倒入______(填仪器名称)中,加热蒸发并用玻璃棒不断搅拌,直到______时(填现象),停止加热.
【问题讨论】
(ⅵ)进行操作⑤前,需先加热,其目的是______,该操作中控制溶液pH=12可确保Mg2+除尽,根据提供的数据计算,此时溶解B中Mg2+物质的量浓度为______.


请根据以上流程,回答相关问题:
(1)操作①的名称:______;操作②名称是:______;
操作③的名称是:______;
操作④需要的玻璃仪器有:______.
(2)参照图2溶解度曲线,欲得到较纯的氯化钾晶体需用少量的______(选填:“热水”,“冷水”)洗涤固体______(选填“A”或“B”).
(3)同学甲提出一些新的方案,对上述操作②后无色溶液进行除杂提纯,其方案如下:
【有关资料】
| 化学式 | BaCO3 | BaSO4 | Ca(OH)2 | MgCO3 | Mg(OH)2 |
| Ksp | 8.1×10一9 | 1.08×10一10 | 1.0×10一4 | 3.5×10一5 | 1.6×10一11 |

(i)若在图3的操作⑤结束后发现溶液B略有浑浊,应采取的措施是______,
(ii)混合液A的主要成分是______.(填化学式)
【检验除杂效果】
(ⅲ)为检验Mg2+、SO42-是否除尽,通常分别取悬浊液A上层清液于两试管中.进行如下实验:
步骤一:检验Mg2+是否除尽.向其中一支试管中加入______溶液(填化学式),如果没有沉淀生成,则Mg2+已除尽.
步骤二:检验SO42-是否除尽.向另一支试管中加入某溶液,如果无有沉淀生成,则SO42-已除尽,效果最好的是______(填字母).
A.Na2 CO3 B.BaCl2 C.CaCl2
【获取纯净氯化钾】
(ⅳ)对溶液B加热并不断滴加l mol?L一1的盐酸溶液,同时用pH试纸检测溶液,直至pH=5时停止加盐酸,得到溶液C.该操作的目的是______.
(ⅴ)将溶液C倒入______(填仪器名称)中,加热蒸发并用玻璃棒不断搅拌,直到______时(填现象),停止加热.
【问题讨论】
(ⅵ)进行操作⑤前,需先加热,其目的是______,该操作中控制溶液pH=12可确保Mg2+除尽,根据提供的数据计算,此时溶解B中Mg2+物质的量浓度为______.

某钠盐溶液可能含有阴离子CO32-、SO32-、SO42-、Cl-、Br-、I-.为鉴定这些离子,分别取少量溶液进行以下实验:(填写如表空格)
| 实验操作与预期现象 | 实验结论 | 判断理由 | |
| 步骤一 | 用pH计测得混合液的pH=9.82 | ①______ | 因为它们水解显碱性 |
| 步骤二 | HCl 后,生成无色无味气体. | ②______ | ③______ |
| 步骤三 | 在步骤二反应后溶液中加 CCl4, 滴加少量氯水,振荡后,CCl4层未变色; | 肯定不存在Br-、I- | ④______ |
| 步骤四 | ⑤______ | 肯定存在SO42- | 因为BaSO4不溶于盐酸. |
| 步骤五 | 在步骤四反应后溶液中加 HNO3 酸化后,再加过量 AgNO3,溶液中析出白色沉淀. | 不能确定Cl-是否存在 | ⑥______ |
重铬酸钾是工业生产和实验室的重要氧化剂,工业上常用铬铁矿为原料生产,实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下,涉及的主要反应是:
6FeO?Cr2O3+24NaOH+7KClO3 12Na2CrO4+3Fe2O3+7KCl+12H2O
12Na2CrO4+3Fe2O3+7KCl+12H2O
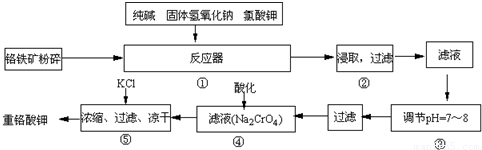
试回答下列问题
(1)指出24Cr在周期表中的位置是______,
(2)NaFeO2能强烈水解,在操作②生成沉淀而除去,写出该反应的化学方程式:______.
(3)操作③调节pH=7~8的原因是______.(用简要的文字和离子方程式说明)
下表是铬酸(H2CrO4)溶液中离子的组成与pH的关系:
(4)操作④酸化的目的是______.
(5)在铬酸(H2CrO4)溶液中,电离出CrO42-的电离平衡常数为K2,电离出Cr2O72-的电离平衡常数为K3,则K2______K3(填>、﹦、<)
(6)上表中铬酸的物质的量浓度为______.(精确到小数点后2位)
0 67193 67201 67207 67211 67217 67219 67223 67229 67231 67237 67243 67247 67249 67253 67259 67261 67267 67271 67273 67277 67279 67283 67285 67287 67288 67289 67291 67292 67293 67295 67297 67301 67303 67307 67309 67313 67319 67321 67327 67331 67333 67337 67343 67349 67351 67357 67361 67363 67369 67373 67379 67387 203614
6FeO?Cr2O3+24NaOH+7KClO3
 12Na2CrO4+3Fe2O3+7KCl+12H2O
12Na2CrO4+3Fe2O3+7KCl+12H2O
试回答下列问题
(1)指出24Cr在周期表中的位置是______,
(2)NaFeO2能强烈水解,在操作②生成沉淀而除去,写出该反应的化学方程式:______.
(3)操作③调节pH=7~8的原因是______.(用简要的文字和离子方程式说明)
下表是铬酸(H2CrO4)溶液中离子的组成与pH的关系:
| pH | C(CrO42-)mol/L | C(HCrO4-)mol/L | C(Cr2O72-)mol/L | C(H2CrO4)mol/L |
| 4 | 0.0003 | 0.104 | 0.448 | |
| 5 | 0.0033 | 0.103 | 0.447 | |
| 6 | 0.0319 | 0.0999 | 0.437 | |
| 7 | 0.2745 | 0.086 | 0.3195 | |
| 8 | 0.902 | 0.0282 | 0.0347 | |
| 9 | 0.996 | 0.0031 | 0.0004 |
(5)在铬酸(H2CrO4)溶液中,电离出CrO42-的电离平衡常数为K2,电离出Cr2O72-的电离平衡常数为K3,则K2______K3(填>、﹦、<)
(6)上表中铬酸的物质的量浓度为______.(精确到小数点后2位)




