煤化工中常需研究不同温度下平衡常数、投料比及热值等问题.
已知:CO(g)+H2O(g) H2(g)+CO2(g)的平衡常数随温度的变化如表:
H2(g)+CO2(g)的平衡常数随温度的变化如表:
试回答下列问题:
(1)上述正向反应是: 反应(选填:放热、吸热).
(2)在800℃发生上述反应,以下表中的物质的量投入恒容反应器,其中向正反应方向移动的有 (选填A、B、C、D、E).
(3)已知在一定温度下:C(s)+CO2(g)  2CO(g)平衡常数K;
2CO(g)平衡常数K;
C(s)+H2O(g) CO(g)+H2(g) 平衡常数K1;
CO(g)+H2(g) 平衡常数K1;
CO(g)+H2O(g) H2(g)+CO2(g) 平衡常数K2,
H2(g)+CO2(g) 平衡常数K2,
则K、K1、K2之间的关系是: .
(4)若在500℃时进行,若CO、H2O的起始浓度均为0.020mol/L,在该条件下,CO的最大转化率为: .
(5)若在800℃进行,设起始时CO和H2O(g)共为5mol,水蒸气的体积分数为x;平衡时CO转化率为y,则y随x变化的函数关系式为:y= .
(6)在VL密闭容器中通入10molCO和10mol水蒸气,在T℃达到平衡,然后急速除去水蒸气(除水蒸气时各物质的物质的量不变),将混合气体燃烧,测得放出的热量为2842kJ(已知CO燃烧热为283kJ/mol,H2燃烧热为286kJ/mol),则T℃平衡常数K= .
0 67143 67151 67157 67161 67167 67169 67173 67179 67181 67187 67193 67197 67199 67203 67209 67211 67217 67221 67223 67227 67229 67233 67235 67237 67238 67239 67241 67242 67243 67245 67247 67251 67253 67257 67259 67263 67269 67271 67277 67281 67283 67287 67293 67299 67301 67307 67311 67313 67319 67323 67329 67337 203614
已知:CO(g)+H2O(g)
 H2(g)+CO2(g)的平衡常数随温度的变化如表:
H2(g)+CO2(g)的平衡常数随温度的变化如表:| 温度/℃ | 400 | 500 | 800 |
| 平衡常数Kc | 9.94 | 9 | 1 |
(1)上述正向反应是: 反应(选填:放热、吸热).
(2)在800℃发生上述反应,以下表中的物质的量投入恒容反应器,其中向正反应方向移动的有 (选填A、B、C、D、E).
| A | B | C | D | E | |
| n(CO2) | 3 | 1 | 1 | 1 | |
| n(H2) | 2 | 1 | 1 | 2 | |
| n(CO) | 1 | 2 | 3 | 0.5 | 3 |
| n(H2O) | 5 | 2 | 3 | 2 | 1 |
 2CO(g)平衡常数K;
2CO(g)平衡常数K;C(s)+H2O(g)
 CO(g)+H2(g) 平衡常数K1;
CO(g)+H2(g) 平衡常数K1;CO(g)+H2O(g)
 H2(g)+CO2(g) 平衡常数K2,
H2(g)+CO2(g) 平衡常数K2,则K、K1、K2之间的关系是: .
(4)若在500℃时进行,若CO、H2O的起始浓度均为0.020mol/L,在该条件下,CO的最大转化率为: .
(5)若在800℃进行,设起始时CO和H2O(g)共为5mol,水蒸气的体积分数为x;平衡时CO转化率为y,则y随x变化的函数关系式为:y= .
(6)在VL密闭容器中通入10molCO和10mol水蒸气,在T℃达到平衡,然后急速除去水蒸气(除水蒸气时各物质的物质的量不变),将混合气体燃烧,测得放出的热量为2842kJ(已知CO燃烧热为283kJ/mol,H2燃烧热为286kJ/mol),则T℃平衡常数K= .
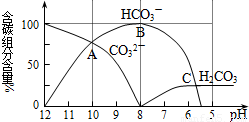
 CH3OH.生产中一些工艺参数如图所示.该反应为 (填“吸热”或“放热”)反应.说明你作出判断的依据 .
CH3OH.生产中一些工艺参数如图所示.该反应为 (填“吸热”或“放热”)反应.说明你作出判断的依据 .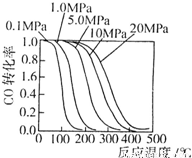

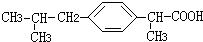
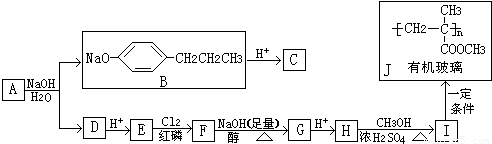
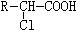 +HCl
+HCl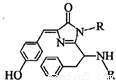
 Mg(OH)2↓+2H+
Mg(OH)2↓+2H+