新切开的苹果在空气中放置一段时间表面会变黄,最终变成褐色,这种现象在食品科学上通常称为“褐变”. 关于苹果褐变的原因有以下两种说法:
A.苹果中的Fe2+被空气中的氧气氧化成了Fe3+
B.苹果中的酚类物质被空气中的氧气氧化了
究竟哪种说法正确,某合作小组同学通过实验进行了探究.
材料:苹果、浓度均为0.1mol?L-1的盐酸、NaCl溶液、NaHCO3溶液、Na2SO3溶液、KSCN溶液、开水
(1)探究1:
(2)探究2:
【查阅文献】
1.苹果中含有多酚和多酚氧化酶,苹果褐变是氧气、酚类、酚氧化酶共同作用生成了醌类物质的缘故.苹果中多酚氧化酶的活性温度为35℃左右、活性pH约为5.5.
2.酚类物质遇FeCl3溶液常发生显色反应而呈现一定颜色,如苯酚显紫色,对苯二酚显绿色,甲基苯酚显蓝色.
该小组将刚削皮的苹果切成七块,进行如下实验验证.请填写下表中相应的结论:
(3)问题与讨论:
①0.1mol?L-1的NaHCO3溶液和Na2SO3溶液的pH相近,Na2SO3溶液却能阻止苹果褐变,可能的原因是:______,反应的离子方程式为:______.
②褐变会影响苹果的品质和口感,试举出家中防止削皮苹果褐变的一种措施:______.
0 66938 66946 66952 66956 66962 66964 66968 66974 66976 66982 66988 66992 66994 66998 67004 67006 67012 67016 67018 67022 67024 67028 67030 67032 67033 67034 67036 67037 67038 67040 67042 67046 67048 67052 67054 67058 67064 67066 67072 67076 67078 67082 67088 67094 67096 67102 67106 67108 67114 67118 67124 67132 203614
A.苹果中的Fe2+被空气中的氧气氧化成了Fe3+
B.苹果中的酚类物质被空气中的氧气氧化了
究竟哪种说法正确,某合作小组同学通过实验进行了探究.
材料:苹果、浓度均为0.1mol?L-1的盐酸、NaCl溶液、NaHCO3溶液、Na2SO3溶液、KSCN溶液、开水
(1)探究1:
| 实验操作 | 实验现象 | 结论 |
| 在“褐变”后的苹果上滴上2~3 滴______溶液 | ______ | 说法A不正确 |
【查阅文献】
1.苹果中含有多酚和多酚氧化酶,苹果褐变是氧气、酚类、酚氧化酶共同作用生成了醌类物质的缘故.苹果中多酚氧化酶的活性温度为35℃左右、活性pH约为5.5.
2.酚类物质遇FeCl3溶液常发生显色反应而呈现一定颜色,如苯酚显紫色,对苯二酚显绿色,甲基苯酚显蓝色.
该小组将刚削皮的苹果切成七块,进行如下实验验证.请填写下表中相应的结论:
| 序号 | 实验步骤 | 现象 | 结论 |
| ① | 在一块上滴加2~3滴FeCl3溶液 | 表面变为绿色 | 苹果中含有酚类物质 |
| ② | 一块放置于空气中 另一块迅速浸入0.1mol?L-1NaCl溶液中 | 表面逐渐褐变 相当长一段时间内,无明显变化 | 苹果褐变与______有关 |
| ③ | 另两块分别立刻放入90℃~95℃的开水和0.1mol?L-1盐酸中浸泡2min后取出,放置于空气中 | 相当长一段时间内,均无明显变化 | 苹果褐变与______有关 |
| ④ | 最后两块分别立刻放入各0.1mol?L-1的NaHCO3溶液和Na2SO3溶液里浸泡2min后取出,放置于空气 | 前者表面逐渐褐变,后者相当长一段时间内,无明显变化 | 亚硫酸钠溶液能阻止苹果褐变 |
①0.1mol?L-1的NaHCO3溶液和Na2SO3溶液的pH相近,Na2SO3溶液却能阻止苹果褐变,可能的原因是:______,反应的离子方程式为:______.
②褐变会影响苹果的品质和口感,试举出家中防止削皮苹果褐变的一种措施:______.
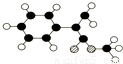
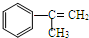 出发来合成M,其合成路线如下:
出发来合成M,其合成路线如下: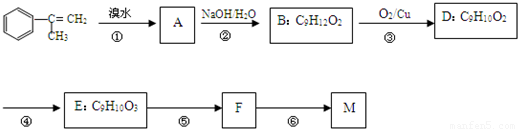
 2O3
2O3