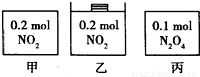
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和如图表示:
下列说法正确的是( )
A.10min内甲容器中反应的平均速率v(A)=0.025mol/
B.由图可知:T1<T2,且该反应为放热反应
C.x=1,若平衡时保持温度不变,改变容器体积平衡不移动
D.T1℃,起始时甲容器中充入0.5molA、1.5molB,平衡时A的转化率为25%
0 66897 66905 66911 66915 66921 66923 66927 66933 66935 66941 66947 66951 66953 66957 66963 66965 66971 66975 66977 66981 66983 66987 66989 66991 66992 66993 66995 66996 66997 66999 67001 67005 67007 67011 67013 67017 67023 67025 67031 67035 67037 67041 67047 67053 67055 67061 67065 67067 67073 67077 67083 67091 203614
| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0,5L | 0,5L | 1,0L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1,5molA 0,5molB | 1,5molA 0,5molB | 6,0molA 2,0molB |

A.10min内甲容器中反应的平均速率v(A)=0.025mol/
B.由图可知:T1<T2,且该反应为放热反应
C.x=1,若平衡时保持温度不变,改变容器体积平衡不移动
D.T1℃,起始时甲容器中充入0.5molA、1.5molB,平衡时A的转化率为25%

 xC(g).
xC(g). ,混合气体的平均摩尔质量增大
,混合气体的平均摩尔质量增大 ,则该反应的化学方程式中n的值是( )
,则该反应的化学方程式中n的值是( )