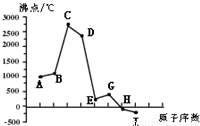
同一周期(短周期)各元素形成单质的沸点变化如下图所示(按原子序数连续递增顺序排列).该周期部分元素氟化物的熔点见下表.
(1)A原子核外共有______种不同运动状态的电子、______种不同能级的电子;
(2)元素C的最高价氧化物对应水化物的电离方程式为______;
(3)解释上表中氟化物熔点差异的原因:______;
(4)在E、G、H三种元素形成的氢化物中,热稳定性最大的是______(填化学式).A、B、C三种原子形成的简单离子的半径由大到小的顺序为______(填离子符号).
| 氟化物 | AF | BF2 | DF4 |
| 熔点/K | 1266 | 1534 | 183 |
(2)元素C的最高价氧化物对应水化物的电离方程式为______;
(3)解释上表中氟化物熔点差异的原因:______;
(4)在E、G、H三种元素形成的氢化物中,热稳定性最大的是______(填化学式).A、B、C三种原子形成的简单离子的半径由大到小的顺序为______(填离子符号).

合成氨工业中原料气(H2、CO的混合气)在进入合成塔前常用醋酸亚铜氨溶液来吸收原料气中的CO:Cu(NH3)2Ac(溶液)+CO(g)?Cu(NH3)2Ac?CO(溶液)+Q kJ(Q>0),吸收CO后的溶液经过适当处理又可以重新生成醋酸亚铜氨.
(1)写出该反应的平衡常数表达式K=______;升高温度K值将______(选填“增大”“减小”“不变”).
(2)必须除去原料气中CO的原因是______,欲充分吸收CO,适宜的条件是______(选填序号)
a.升高温度 b.增大压强 c.增大醋酸亚铜氨溶液浓度
吸收CO时,溶液中Cu(NH3)2Ac和Cu(NH3)2Ac?CO的浓度(mol/L)变化情况如下:
(3)前30min Cu(NH3)2Ac的平均反应速率为______;
(4)60min时改变的条件可能是______.
0 66805 66813 66819 66823 66829 66831 66835 66841 66843 66849 66855 66859 66861 66865 66871 66873 66879 66883 66885 66889 66891 66895 66897 66899 66900 66901 66903 66904 66905 66907 66909 66913 66915 66919 66921 66925 66931 66933 66939 66943 66945 66949 66955 66961 66963 66969 66973 66975 66981 66985 66991 66999 203614
(1)写出该反应的平衡常数表达式K=______;升高温度K值将______(选填“增大”“减小”“不变”).
(2)必须除去原料气中CO的原因是______,欲充分吸收CO,适宜的条件是______(选填序号)
a.升高温度 b.增大压强 c.增大醋酸亚铜氨溶液浓度
吸收CO时,溶液中Cu(NH3)2Ac和Cu(NH3)2Ac?CO的浓度(mol/L)变化情况如下:
| 0min | 30min | 45min | 60min | 90min | |
| Cu(NH3)2Ac | 2.0 | 1.2 | 0.9 | 0.9 | 1.8 |
| Cu(NH3)2Ac?CO | a | 1.1 | 1.1 | 0.2 |
(4)60min时改变的条件可能是______.


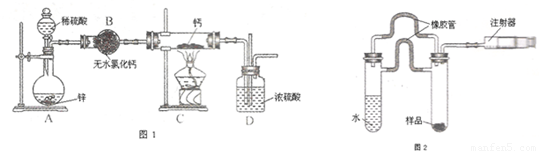
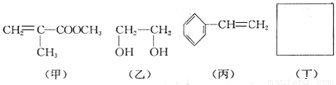
 A
A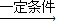 B→C
B→C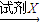 D
D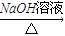 乙
乙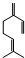 ,一分子该物质与一分子溴发生加成反应的产物(只考虑位置异构)理论上最多有______种
,一分子该物质与一分子溴发生加成反应的产物(只考虑位置异构)理论上最多有______种