一定温度范围内用氯化钠熔浸钾长石(主要成份为KAlSi3O8)可制得氯化钾,主要反应是:NaCl(l)+KAlSi3O8(s)?KCl(l)+NaAlSi3O8(s).
(1)氯化钠的电子式是 .
(2)上述反应涉及的元素中,原子半径最大的是 .
(3)上述反应涉及的位于同一周期的几种元素中,有一种元素的最高价氧化物的水化物和其余元素的最价氧化物的水化物均能发生反应,该元素是 .
(4)某兴趣小组为研究上述反应中钾元素的熔出率(液体中钾元素的质量占样品质量的百分率)与温度的关系,进行实验(保持其它条件不变),获得如下数据:
①分析数据可以得出,氯化钠熔浸钾长石是 (填“放热”或“吸热”)反应.
②950℃时,欲提高熔出钾的速率可以采取的措施是 (填序号).
a.充分搅拌
b.延长反应时间
c.增大反应体系的压强
d.将钾长石粉粹成更小的颗粒
(5)该方法制得KCl提纯后可用来冶炼金属钾.反应Na(l)+KCl(l)?NaCl(l)+K(g)是工业上冶炼金属钾常用的方法,用平衡原理解释该方法可行的原因是 .
0 66792 66800 66806 66810 66816 66818 66822 66828 66830 66836 66842 66846 66848 66852 66858 66860 66866 66870 66872 66876 66878 66882 66884 66886 66887 66888 66890 66891 66892 66894 66896 66900 66902 66906 66908 66912 66918 66920 66926 66930 66932 66936 66942 66948 66950 66956 66960 66962 66968 66972 66978 66986 203614
(1)氯化钠的电子式是 .
(2)上述反应涉及的元素中,原子半径最大的是 .
(3)上述反应涉及的位于同一周期的几种元素中,有一种元素的最高价氧化物的水化物和其余元素的最价氧化物的水化物均能发生反应,该元素是 .
(4)某兴趣小组为研究上述反应中钾元素的熔出率(液体中钾元素的质量占样品质量的百分率)与温度的关系,进行实验(保持其它条件不变),获得如下数据:
时间(h) 熔出率 温度 | 1.5 | 2.5 | 3.0 | 3.5 | 4.0 | 5.0 |
| 800℃ | 0.054 | 0.091 | 0.127 | 0.149 | 0.165 | 0.183 |
| 830℃ | 0.481 | 0.575 | 0.626 | 0.669 | 0.685 | 0.687 |
| 860℃ | 0.515 | 0.624 | 0.671 | 0.690 | 0.689 | 0.690 |
| 950℃ | 0.669 | 0.714 | 0.710 | 0.714 | 0.714 | -- |
②950℃时,欲提高熔出钾的速率可以采取的措施是 (填序号).
a.充分搅拌
b.延长反应时间
c.增大反应体系的压强
d.将钾长石粉粹成更小的颗粒
(5)该方法制得KCl提纯后可用来冶炼金属钾.反应Na(l)+KCl(l)?NaCl(l)+K(g)是工业上冶炼金属钾常用的方法,用平衡原理解释该方法可行的原因是 .
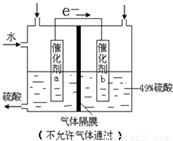
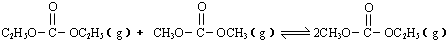 是碳酸甲乙酯的工业生产原理.如图是投料比[
是碳酸甲乙酯的工业生产原理.如图是投料比[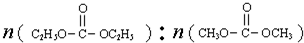 ]分别为3:1和1:1、反应物的总物质的量相同时,
]分别为3:1和1:1、反应物的总物质的量相同时,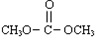 的平衡转化率与温度的关系曲线.下列说法正确的是( )
的平衡转化率与温度的关系曲线.下列说法正确的是( )

 RCO18OR“+R'OH
RCO18OR“+R'OH