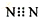某同学进行试验探究时,欲配制1.0mol?L-1Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2?8H2O试剂(化学式量:315).在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在大量未溶物.为探究原因,该同学查得Ba(OH)2?8H2O在283K、293K和303K时的溶解度(g/100g H2O)分别为2.5、3.9和5.6.
(1)烧杯中未溶物仅为BaCO3,理由是 .
(2)假设试剂由大量Ba(OH)2?8H2O和少量BaCO3组成,设计试验方案,进行成分检验,在答题卡上写出实验步骤、预期现象和结论.(不考虑结晶水的检验;室温时BaCO3饱和溶液的pH=9.6)
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
(3)将试剂初步提纯后,准确测定其中Ba(OH)2?8H2O的含量.实验如下:
①配制250ml 约0.1mol?L-1Ba(OH)2?8H2O溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水, ,将溶液转入 ,洗涤,定容,摇匀.
②滴定:准确量取25.00ml所配制Ba(OH)2溶液于锥形瓶中,滴加指示剂,将 (填“0.020”、“0.05”、“0.1980”或“1.5”)mol?L-1盐酸装入50ml酸式滴定管,滴定至终点,记录数据.重复滴定2次.平均消耗盐酸Vml.
③计算Ba(OH)2?8H2O的质量分数= (只列出算式,不做运算)
(4)室温下, (填“能”或“不能”) 配制1.0mol?L-1Ba(OH)2溶液.
0 66778 66786 66792 66796 66802 66804 66808 66814 66816 66822 66828 66832 66834 66838 66844 66846 66852 66856 66858 66862 66864 66868 66870 66872 66873 66874 66876 66877 66878 66880 66882 66886 66888 66892 66894 66898 66904 66906 66912 66916 66918 66922 66928 66934 66936 66942 66946 66948 66954 66958 66964 66972 203614
(1)烧杯中未溶物仅为BaCO3,理由是 .
(2)假设试剂由大量Ba(OH)2?8H2O和少量BaCO3组成,设计试验方案,进行成分检验,在答题卡上写出实验步骤、预期现象和结论.(不考虑结晶水的检验;室温时BaCO3饱和溶液的pH=9.6)
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀. | |
| 步骤2:取适量滤液于试管中,滴加稀硫酸. | |
| 步骤3:取适量步骤1中的沉淀于是试管中, | |
| 步骤4: |
①配制250ml 约0.1mol?L-1Ba(OH)2?8H2O溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水, ,将溶液转入 ,洗涤,定容,摇匀.
②滴定:准确量取25.00ml所配制Ba(OH)2溶液于锥形瓶中,滴加指示剂,将 (填“0.020”、“0.05”、“0.1980”或“1.5”)mol?L-1盐酸装入50ml酸式滴定管,滴定至终点,记录数据.重复滴定2次.平均消耗盐酸Vml.
③计算Ba(OH)2?8H2O的质量分数= (只列出算式,不做运算)
(4)室温下, (填“能”或“不能”) 配制1.0mol?L-1Ba(OH)2溶液.
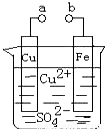
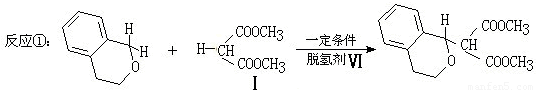
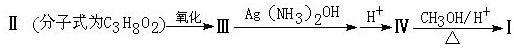
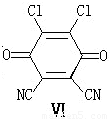 )分子获得2个氢原子后,转变成1个芳香族化合物分子,该芳香族化合物分子的结构简式为 .
)分子获得2个氢原子后,转变成1个芳香族化合物分子,该芳香族化合物分子的结构简式为 .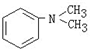 与1分子
与1分子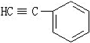 在一定条件下可发生类似①的反应,其产物分子的结构简式为 ;1mol该产物最多可与 molH2发生加成反应.
在一定条件下可发生类似①的反应,其产物分子的结构简式为 ;1mol该产物最多可与 molH2发生加成反应.