蛋白质主要由氨基酸组成,平均含氮量为16%左右.通用的蛋白质测试方法--凯式定氮法--是通过测出含氮量来估算蛋白质含量,主要原理为:将食品与硫酸和催化剂一起加热,使蛋白质分解,分解的氨用硼酸吸收后再以盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,即为蛋白质含量.
已知:1mol氨基能产生1mol氨气;
2NH3+4H3BO3→(NH4)2B4O7+5H2O;
(NH4)2B4O7+2HCl+5H2O→2NH4Cl+4H3BO3
某兴趣小组进行了如下实验:
步骤I 称取样品1.500g.
步骤II (略)
步骤Ⅲ共得到1L吸收了氨的硼酸样品溶液,从中移取10.00mL于250mL锥形瓶中,加入少量水和指示剂,用0.010mol/L的盐酸滴定至终点.
(1)根据步骤Ⅲ填空:
①滴定管用蒸馏水洗涤后,直接加入盐酸进行滴定,则测得样品中氮的质量分数______(填“偏高”、“偏低”或“无影响”).
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去盐酸的体积______ (填“偏大”、“偏小”或“无影响”).
③滴定时边滴边摇动锥形瓶,眼睛应观察______.
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
(2)滴定结果如下表所示:
该样品中氮的质量分数为______.
已知:1mol氨基能产生1mol氨气;
2NH3+4H3BO3→(NH4)2B4O7+5H2O;
(NH4)2B4O7+2HCl+5H2O→2NH4Cl+4H3BO3
某兴趣小组进行了如下实验:
步骤I 称取样品1.500g.
步骤II (略)
步骤Ⅲ共得到1L吸收了氨的硼酸样品溶液,从中移取10.00mL于250mL锥形瓶中,加入少量水和指示剂,用0.010mol/L的盐酸滴定至终点.
(1)根据步骤Ⅲ填空:
①滴定管用蒸馏水洗涤后,直接加入盐酸进行滴定,则测得样品中氮的质量分数______(填“偏高”、“偏低”或“无影响”).
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去盐酸的体积______ (填“偏大”、“偏小”或“无影响”).
③滴定时边滴边摇动锥形瓶,眼睛应观察______.
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
(2)滴定结果如下表所示:
| 滴定次数 | 待测溶液的体积(mL) | 标准溶液的体积 | |
| 初读数(mL) | 末读数(mL) | ||
| 1 | 10.00 | 0.00 | 14.90 |
| 2 | 10.00 | 0.10 | 15.05 |
| 3 | 10.00 | 0.50 | 17.00 |
卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子.若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁.
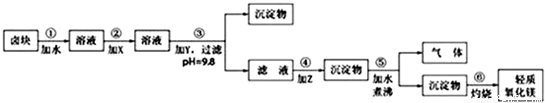
若要求产品尽量不含杂质,而且生产成本较低,根据表1和表2提供的资料,填写空白:
表1生成氢氧化物沉淀的pH
Fe2+氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去.
表2原料价格表
(1)在步骤②中加入的试剂X,最佳的选择是______,其作用是______;
(2)在步骤③中加入的试剂应是______;之所以要控制pH=9.8,其目的是______;
(3)在步骤④中加入的试剂Z应是______;
(4)在步骤⑤中发生的反应是______.

若要求产品尽量不含杂质,而且生产成本较低,根据表1和表2提供的资料,填写空白:
表1生成氢氧化物沉淀的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6* |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
表2原料价格表
| 物质 | 价格/元?吨-1 |
| 漂液(含25.2%NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
| 烧碱(含98%NaOH) | 2100 |
| 纯碱(含99.5%Na2CO3) | 600 |
(2)在步骤③中加入的试剂应是______;之所以要控制pH=9.8,其目的是______;
(3)在步骤④中加入的试剂Z应是______;
(4)在步骤⑤中发生的反应是______.
第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需要的能量.下表是部分元素原子的第一电离能I1:(单位)
回答下列问题:
(1)从表中数据可知,同一主族元素原子的第一电离能I1变化规律是______.说明同一主族元素______能力从上到下逐渐增强.
(2)从表中数据预测Ge元素第一电离能x的取值范围______.
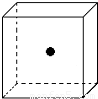
(3)SiC是原子晶体,其结构类似金刚石,为C、Si两原子依次相同排列的正四面体空间网状结构.如图为一个正方体,其中心为Si原子,试在正方体的顶点画出与Si(用 )最近的C(用 表示)的位置.
)最近的C(用 表示)的位置.
| H | He | ||||||
| 1.3120 | 0.3723 | ||||||
| Li | Be | B | C | N | O | F | Ne |
| 0.5203 | 0.8995 | 0.8001 | 1.0864 | 1.4023 | 1.3140 | 1.6810 | 2.0807 |
| Na | Mg | Al | Si | P | S | Cl | Ar |
| 0.4958 | 0.7377 | 0.5776 | 0.7865 | 1.0118 | 0.9996 | 1.2511 | 1.5205 |
| K | Ca | Ga | Ge | As | Se | Br | Kr |
| 0.4189 | 0.5898 | 0.5788 | x | 0.9440 | 0.9409 | 1.1399 | 1.3507 |
| Rb | Sr | In | Sn | Sb | Te | I | Xe |
| 0.4030 | 0.5495 | 0.5583 | 0.7086 | 0.8316 | 0.8693 | 1.0084 | 1.1704 |
| Cs | Ba | Tl | Pb | Bi | Po | At | |
(1)从表中数据可知,同一主族元素原子的第一电离能I1变化规律是______.说明同一主族元素______能力从上到下逐渐增强.
(2)从表中数据预测Ge元素第一电离能x的取值范围______.
(3)SiC是原子晶体,其结构类似金刚石,为C、Si两原子依次相同排列的正四面体空间网状结构.如图为一个正方体,其中心为Si原子,试在正方体的顶点画出与Si(用
 )最近的C(用 表示)的位置.
)最近的C(用 表示)的位置.
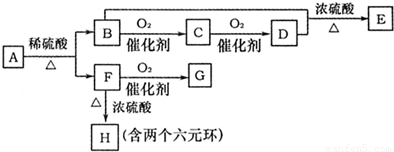
分析下表中各项的排布规律,按此规律排布第26项应为( )
A.C7H16
B.C7H14O2
C.C8H18
D.C8H18O
0 66691 66699 66705 66709 66715 66717 66721 66727 66729 66735 66741 66745 66747 66751 66757 66759 66765 66769 66771 66775 66777 66781 66783 66785 66786 66787 66789 66790 66791 66793 66795 66799 66801 66805 66807 66811 66817 66819 66825 66829 66831 66835 66841 66847 66849 66855 66859 66861 66867 66871 66877 66885 203614
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| C2H4 | C2H6 | C2H6O | C2H6O2 | C3H6 | C3H8 | C3H8O | C3H8O2 | C4H8 | C4H10 |
A.C7H16
B.C7H14O2
C.C8H18
D.C8H18O
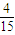 .
.
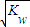 mol?L-1
mol?L-1