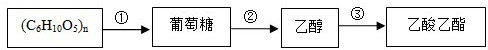
Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好PH和 浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物.现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响.
[实验设计]控制p-CP的初始浓度相同,恒定实验温度在298 K或313 K(其余实验条件见下表),设计如下对比试验.
(1)请完成以下实验设计表(表中不要留空格).
[数据处理]实验测得p-CP的浓度随时间变化的关系如图.
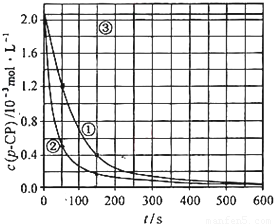
(2)请根据如图实验①曲线,计算降解反应在50~150s内的反应速率:(p-CP)= mol?L-1?s-1
[解释与结论]
(3)实验①、②表明温度升高,降解反应速率增大.但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:
(4)实验③得出的结论是: PH等于10时,
[思考与交流]
(5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来.根据上图中的信息,给出一种迅速停止反应的方法: .
[实验设计]控制p-CP的初始浓度相同,恒定实验温度在298 K或313 K(其余实验条件见下表),设计如下对比试验.
(1)请完成以下实验设计表(表中不要留空格).
| 实验编号 | 实验目的 | T/K | pH | c/10-3mol.L-1 | |
| H2O | Fe2- | ||||
| (1) | 为以下实验作参照 | 298 | 3 | 6.0 | 0.30 |
| (2) | 探究温度对降解反应速的影响率 | ||||
| (3) | 298 | 10 | 6.0 | 0.30 | |

(2)请根据如图实验①曲线,计算降解反应在50~150s内的反应速率:(p-CP)= mol?L-1?s-1
[解释与结论]
(3)实验①、②表明温度升高,降解反应速率增大.但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:
(4)实验③得出的结论是: PH等于10时,
[思考与交流]
(5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来.根据上图中的信息,给出一种迅速停止反应的方法: .
在一容积为2L的恒容密闭容器中加入0.2mol CO和0.4mol H2,发生如下反应:( )
CO(g)+2H2(g)?CH3OH(g) 实验测得300℃和500℃下,甲醇的物质的量随时间的变化如下表所示,下列说法正确的是
A.该反应的焓变△H>0,升高温度K增大
B.300℃时,0~20 min H2的平均反应速率 ν(H2)=0.003mol/
C.采取加压、增大H2浓度、加入催化剂的措施都能提高CO的转化率
D.500℃下,向该容器中初始加入0.1 mol CO和0.3 mol H2,依据现有数据可计算出反应达平衡后甲醇的浓度
0 66656 66664 66670 66674 66680 66682 66686 66692 66694 66700 66706 66710 66712 66716 66722 66724 66730 66734 66736 66740 66742 66746 66748 66750 66751 66752 66754 66755 66756 66758 66760 66764 66766 66770 66772 66776 66782 66784 66790 66794 66796 66800 66806 66812 66814 66820 66824 66826 66832 66836 66842 66850 203614
CO(g)+2H2(g)?CH3OH(g) 实验测得300℃和500℃下,甲醇的物质的量随时间的变化如下表所示,下列说法正确的是
甲醇物 时间 质的量 温度 | 10min | 20min | 30min | 40min | 50min | 60min |
| 300℃ | 0.080 | 0.120 | 0.150 | 0.168 | 0.180 | 0.180 |
| 500℃ | 0.120 | 0.150 | 0.156 | 0.160 | 0.160 | 0.160 |
A.该反应的焓变△H>0,升高温度K增大
B.300℃时,0~20 min H2的平均反应速率 ν(H2)=0.003mol/
C.采取加压、增大H2浓度、加入催化剂的措施都能提高CO的转化率
D.500℃下,向该容器中初始加入0.1 mol CO和0.3 mol H2,依据现有数据可计算出反应达平衡后甲醇的浓度
 O2(g)=FeO(s)△H=-272.0KJ?mol-1 ①
O2(g)=FeO(s)△H=-272.0KJ?mol-1 ① O2(g)=X2O3(s)△H=-1675.7KJ?mol-1 ②
O2(g)=X2O3(s)△H=-1675.7KJ?mol-1 ②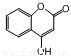 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成: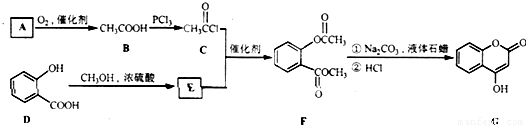
 Fe2O3+3H2
Fe2O3+3H2 2Fe+Al2O3
2Fe+Al2O3