(14分)工业制硝酸的主要反应是4NH3(g)+5O2(g)  4NO(g)+6H2O(g)ΔH=-akJ/mol(a﹥0)
4NO(g)+6H2O(g)ΔH=-akJ/mol(a﹥0)
(1)如果将4molNH3和5molO2放入容器中,达到平衡时,放出热量0.8akJ,则反应时转移的电子数为
mol
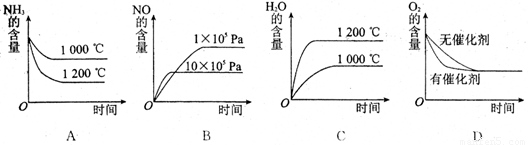
(2)若其他条件不变,下列关系图中错误的是 (选填序号)
(3)t℃时,在容积固定的密闭容器中发生上述反应,容器内各物质的浓度如下表
|
浓度(mol/L) 时间(min) |
c(NH3) |
c(O2) |
c(NO) |
c(H2O) |
|
起 始 |
4.0 |
5.5 |
0 |
0 |
|
第2min |
3.2 |
x |
0.8 |
1.2 |
|
第4min |
2.0 |
3.0 |
2.0 |
3.0 |
|
第6min |
2.0 |
3.0 |
2.0 |
3.0 |
①反应在第2mim到第4mim时,反应速率v(O2)=
②第2min时改变了条件,改变的条件可能是
A.升高温度 B.使用了催化剂 C.减小压强 D.增加了生成物
③在相同的温度下,起始向容器中加入NH3、O2、NO和H2O(g)的浓度都为1mol/L,则该反应将向 _______方向进行(填“正反应”.“逆反应”.“不移动”)
(4)工业上用水吸收二氧化氮生产硝酸,生成的NO2气体经过多次氧化、吸收的循环操作使其充分转化为硝酸(假定上述过程中无其它损失),现有23吨NO2经过2次氧化吸收得到20℅的稀硝酸 吨。
(5)成品硝酸的浓度为60%~70%,为了制浓硝酸,常用Mg(NO3)2作吸水剂,然后进行蒸馏,不用CaCl2或MgCl2作吸水剂的原因是__________________________________________
氯化亚铁溶液中滴加硫氰化钾溶液,再滴加双氧水,立即出现血红色,后红色又褪去呈黄色并伴有气泡产生,针对该实验现象,某实验小组的同学进行了探究
一、现象分析
假设A:气泡是H2O2分解产生的O2
假设B:气泡是KSCN被氧化为N2、SO2、CO2等
假设C:红色褪去的原因是KSCN被氧化成了其它物质
二、实验探究
探究1
|
实验操作 |
实验现象 |
结论 |
|
①1mL 0.1mol/L的FeCl2溶液中加2滴KSCN溶液 |
溶液不变红 |
Fe2+遇SCN-不变红 |
|
②向①的溶液中加3%的H2O21滴并振荡 |
立即出现血红色 振荡后不褪色 |
加入H2O2后溶液中 出现了 (离子符号) |
|
③向②的溶液中继续加H2O2溶液 |
溶液中出现大量气泡 血红色褪去 |
|
|
④用带火星的木条检验③中的气体 |
木条复燃 |
则假设 成立 |
探究2
|
实验操作 |
实验现象 |
结论 |
|
①取2ml KSCN溶液向其中加入几滴BaCl2溶液和稀盐酸 |
无明显现象 |
|
|
②向①所得的溶液中滴加3%的H2O2 |
溶液中出现白色沉淀并有少量气泡
|
白色沉淀为BaSO4
|
|
③将6%的H2O2溶液加入KSCN固体中,生成的气体依次通过品红溶液,酸性KMnO4溶液和澄清的石灰水 |
|
KSCN被H2O2氧化生成了SO2和CO2气体 |
三、问题与讨论
(1)探究1中,H2O2分解速度很快的原因
(2)探究1中,说明还原性Fe2+ SCN-
(3)探究2中,酸性KMnO4溶液的作用是
能证明生成了CO2的现象是
(4)若SCN -被H2O2氧化得到N2、SO2、CO2和SO42-,且SO2与SO42-的物质的量比为1:1,试写出该反应的离子方程式
科学工作者发现另一种“足球分子”N60,它的结构与C60相似。下列说法正确的是
A.N60和C60互为同素异形体 B.N60是一种新型化合物
C.N60和N2是同系物 D.N60和14N都是氮的同系物
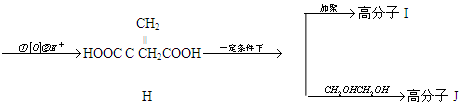
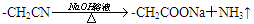
 6Cu+SO2↑反应中,说法正确的是
6Cu+SO2↑反应中,说法正确的是