在80℃时,将0.40mol的N24气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4?2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:
(1)计算20s一40s内用N2O4表示的平均反应速率为______mol?L-1?S-1;
(2)计算在80℃时该反应的平衡常数K=______(请注明单位).
(3)反应进行至100s后将反应混合物的温度降低,混合气体的颜色(填“变浅”.“变深”或“不变”)______;
(4)要增大该反应的K值,可采取的措施有(填序号)______:
A.增大N2O4的起始浓度 B.向混合气体中通入NO2 C.使用高效催化剂 D.升高温度
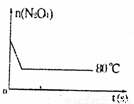
(5)如图是80℃时容器中N24物质的量的变化曲线,请在该图中补画出该反应在60℃时N24物质的量的变化曲线.
0 66469 66477 66483 66487 66493 66495 66499 66505 66507 66513 66519 66523 66525 66529 66535 66537 66543 66547 66549 66553 66555 66559 66561 66563 66564 66565 66567 66568 66569 66571 66573 66577 66579 66583 66585 66589 66595 66597 66603 66607 66609 66613 66619 66625 66627 66633 66637 66639 66645 66649 66655 66663 203614
| 时间(s) n(mol) | 20 | 40 | 60 | 80 | 100 | |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(2)计算在80℃时该反应的平衡常数K=______(请注明单位).
(3)反应进行至100s后将反应混合物的温度降低,混合气体的颜色(填“变浅”.“变深”或“不变”)______;
(4)要增大该反应的K值,可采取的措施有(填序号)______:
A.增大N2O4的起始浓度 B.向混合气体中通入NO2 C.使用高效催化剂 D.升高温度
(5)如图是80℃时容器中N24物质的量的变化曲线,请在该图中补画出该反应在60℃时N24物质的量的变化曲线.