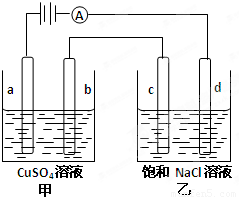
将洁净的金属片Fe、Zn、A、B 分别与Cu用导线连接浸在合适的电解质溶液里.实验并记录电压指针的移动方向和电压表的读数如下表所示:
根据以上实验记录,完成以下填空:
(1)构成两电极的金属活动性相差越大,电压表的读数越______(填“大”、“小”).
Zn、A、B三种金属活动性由强到弱的顺序是______.
(2)Cu与A组成的原电池,______为负极,此电极反应式为(失去电子数用ne-表示______.
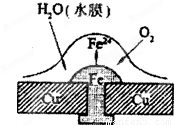
(3)A、B形成合金,露置在潮湿空气中,______先被腐蚀.
| 金属 | 电子流动方向 | 电压/V |
| Fe | Fe→Cu | +0.78 |
| Zn | Zn→Cu | +1.10 |
| A | Cu→A | -0.15 |
| B | B→Cu | +0.3 |
(1)构成两电极的金属活动性相差越大,电压表的读数越______(填“大”、“小”).
Zn、A、B三种金属活动性由强到弱的顺序是______.
(2)Cu与A组成的原电池,______为负极,此电极反应式为(失去电子数用ne-表示______.
(3)A、B形成合金,露置在潮湿空气中,______先被腐蚀.
已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不不反应).某化学兴趣小组在实验室条件下用以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定.
步骤一:电解精制:
请回答以下问题:
Ⅰ.电解时,粗铜应与电源的______极相连.阴极上的电极反应式为______
电解过程中,硫酸铜的浓度会变小,原因是锌,铁与硫酸铜发生置换反应.
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:
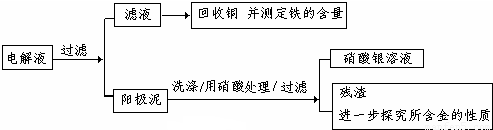
(1)阳极泥的综合利用:
Ⅱ.稀硝酸处理阳极泥得到硝酸银稀溶液,请你写出该步反应的化学方程式:______
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的知识,以下是他们获取的一些极其重要的信息:
Ⅲ.从平衡常数的大小可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与盐酸按体积比1:3的混合物),请你简要解释金能够溶于王水的原因:______
(2)滤液含量的测定:
以下是该小组探究滤液的一个实验流程:
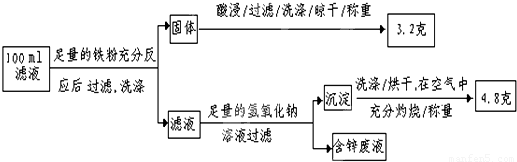
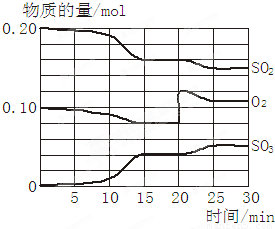
Ⅳ.则100mL滤液中Cu2+ 的浓度为______mol?L-1,
Ⅴ.则100mL滤液中Fe2+的浓度为______mol?L-1.
0 66258 66266 66272 66276 66282 66284 66288 66294 66296 66302 66308 66312 66314 66318 66324 66326 66332 66336 66338 66342 66344 66348 66350 66352 66353 66354 66356 66357 66358 66360 66362 66366 66368 66372 66374 66378 66384 66386 66392 66396 66398 66402 66408 66414 66416 66422 66426 66428 66434 66438 66444 66452 203614
步骤一:电解精制:
请回答以下问题:
Ⅰ.电解时,粗铜应与电源的______极相连.阴极上的电极反应式为______
电解过程中,硫酸铜的浓度会变小,原因是锌,铁与硫酸铜发生置换反应.
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:

(1)阳极泥的综合利用:
Ⅱ.稀硝酸处理阳极泥得到硝酸银稀溶液,请你写出该步反应的化学方程式:______
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的知识,以下是他们获取的一些极其重要的信息:
| 序号 | 反应 | 平衡常数 |
| ① | Au+6HNO3(浓)?Au(NO3)3+3NO2+3H2O | <<1 |
| ② | Au3++4Cl-?AuCl4- | >>1 |
(2)滤液含量的测定:
以下是该小组探究滤液的一个实验流程:

Ⅳ.则100mL滤液中Cu2+ 的浓度为______mol?L-1,
Ⅴ.则100mL滤液中Fe2+的浓度为______mol?L-1.
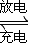 3Zn(OH)2+2Fe(OH)3+4KOH下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH下列叙述不正确的是( )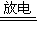 Zn(OH)2
Zn(OH)2 FeO42-+4H2O
FeO42-+4H2O