控制变量法是研究化学变化规侓的重要思想方法.请仔细观察下表中50mL稀盐酸和1g碳酸钙反应的实验数据:
分析并回答下列问题:
(1)本反应属于 反应(填吸热或放热).反应的离子方程式为 .
(2)实验6和7表明, 对反应速率有影响, 反应速率越快,能表明同一规律的实验还有 (填实验序号).
(3)根据实验1、3、4、6、8可以得出条件对反应速率的影响规律是 .
(4)本实验中影响反应速率的其它因素还有 ,能表明这一规律的实验序号是1、2与 .
0 66105 66113 66119 66123 66129 66131 66135 66141 66143 66149 66155 66159 66161 66165 66171 66173 66179 66183 66185 66189 66191 66195 66197 66199 66200 66201 66203 66204 66205 66207 66209 66213 66215 66219 66221 66225 66231 66233 66239 66243 66245 66249 66255 66261 66263 66269 66273 66275 66281 66285 66291 66299 203614
| 实验 序号 | 碳酸钙 状态 | c(HCl) /mol?L-1 | 溶液温度/℃ | 碳酸钙消失 时间/s | |
| 反应前 | 反应后 | ||||
| 1 | 粒状 | 0.5 | 20 | 39 | 400 |
| 2 | 粉末 | 0.5 | 20 | 40 | 60 |
| 3 | 粒状 | 0.6 | 20 | 41 | 280 |
| 4 | 粒状 | 0.8 | 20 | 40 | 200 |
| 5 | 粉末 | 0.8 | 20 | 40 | 30 |
| 6 | 粒状 | 1.0 | 20 | 40 | 120 |
| 7 | 粒状 | 1.0 | 30 | 50 | 40 |
| 8 | 粒状 | 1.2 | 20 | 40 | 90 |
| 9 | 粒状 | 1.2 | 25 | 45 | 40 |
(1)本反应属于 反应(填吸热或放热).反应的离子方程式为 .
(2)实验6和7表明, 对反应速率有影响, 反应速率越快,能表明同一规律的实验还有 (填实验序号).
(3)根据实验1、3、4、6、8可以得出条件对反应速率的影响规律是 .
(4)本实验中影响反应速率的其它因素还有 ,能表明这一规律的实验序号是1、2与 .
 2CH3COOH.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
2CH3COOH.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.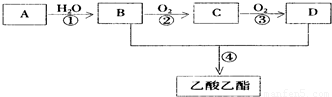
 O2(g)=2H2O(l)+CO(g)△H1
O2(g)=2H2O(l)+CO(g)△H1 O2(g)=SO3(s)△H2
O2(g)=SO3(s)△H2 v(A)
v(A) v(C)
v(C) v(C)
v(C)