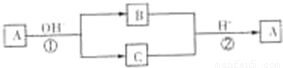
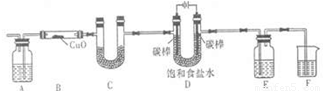
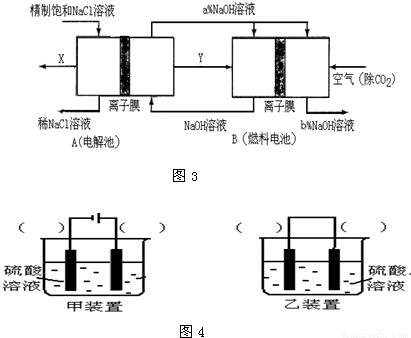
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序为 .
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是 .
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: .
(4)⑥的单质与⑤的最高价氧化物的水化物发生反应的化学方程式: .
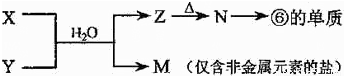
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:X溶液与Y溶液反应的离子方程式为 .
0 66014 66022 66028 66032 66038 66040 66044 66050 66052 66058 66064 66068 66070 66074 66080 66082 66088 66092 66094 66098 66100 66104 66106 66108 66109 66110 66112 66113 66114 66116 66118 66122 66124 66128 66130 66134 66140 66142 66148 66152 66154 66158 66164 66170 66172 66178 66182 66184 66190 66194 66200 66208 203614
| 族 周期 | IA | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是 .
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: .
(4)⑥的单质与⑤的最高价氧化物的水化物发生反应的化学方程式: .
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:X溶液与Y溶液反应的离子方程式为 .