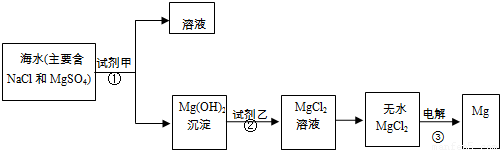
如表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )
A.L2+与R2-的核外电子数相等
B.L与T形成的化合物具有两性
C.氢化物的稳定性为H2T<H2R
D.L和Q失电子能力大小比较是Q<L
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.134 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.L2+与R2-的核外电子数相等
B.L与T形成的化合物具有两性
C.氢化物的稳定性为H2T<H2R
D.L和Q失电子能力大小比较是Q<L
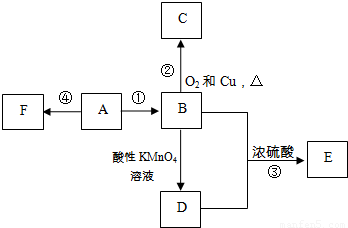
(现有部分短周期元素的性质或原子结构如表:
(1)写出B元素在元素周期表中的位置 .
(2)写出C元素气态氢化物的电子式 .
(3)元素D与元素B相比,非金属性较强的是 (用元素符号表示),下列叙述中能证明这一事实的是 (填数字序号).
①常温下D的单质和B的单质状态不同
②D的气态氢化物比B的气态氢化物稳定
③B元素最高价氧化物的水化物酸性强于D元素最高价氧化物的水化物酸性
(4)由表中元素形成的常见物质X、Y、Z、M、N存在以下转化关系:
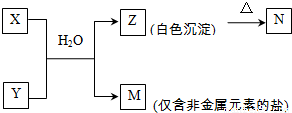
①N的化学式为 .
②X溶液与Y溶液反应的离子方程式为 .
0 65899 65907 65913 65917 65923 65925 65929 65935 65937 65943 65949 65953 65955 65959 65965 65967 65973 65977 65979 65983 65985 65989 65991 65993 65994 65995 65997 65998 65999 66001 66003 66007 66009 66013 66015 66019 66025 66027 66033 66037 66039 66043 66049 66055 66057 66063 66067 66069 66075 66079 66085 66093 203614
| 元素编号 | 元素性质或原子结构 |
| A | 该元素的一种原子,原子核中没有中子 |
| B | 有三个电子层,且K、M层电子数之和等于L层电子数 |
| C | 单质为双原子分子,其氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
| E | 1mol E的单质与足量的稀盐酸反应,可得到氢气33.6L (标准状况) |
(2)写出C元素气态氢化物的电子式 .
(3)元素D与元素B相比,非金属性较强的是 (用元素符号表示),下列叙述中能证明这一事实的是 (填数字序号).
①常温下D的单质和B的单质状态不同
②D的气态氢化物比B的气态氢化物稳定
③B元素最高价氧化物的水化物酸性强于D元素最高价氧化物的水化物酸性
(4)由表中元素形成的常见物质X、Y、Z、M、N存在以下转化关系:

①N的化学式为 .
②X溶液与Y溶液反应的离子方程式为 .