某化学反应中,设反应物的总能量为E1,生成物的总能量为E2.
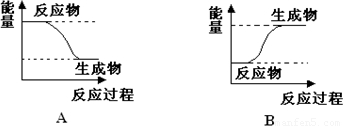
(1)若E1>E2,则该反应为 (填“放热”或“吸热”)反应.该反应可用图 (填“A”或“B”)表示.
(2)若E1<E2,则该反应为 (填“放热”或“吸热”)反应.该反应可用图 (填“A”或“B”)表示.
(3)太阳能的开发和利用是21世纪的一个重要课题.
①利用储能介质储存太阳能的原理是白天在太阳照射下,某种盐熔化,吸收热量;晚间熔盐释放出相应能量,从而使室温得以调节.已知下列数据:
其中最适宜作储能介质的是 (填字母).
A.CaCL2?6H2O B、Na2SO4?10H2O C.Na2HPO4?12H2O D、Na2S2O3?5H2O
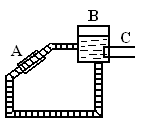
②右图是一种太阳能热水器的示意图,图中A是集热器,B是储水容器,C是供阴天时加热的辅助电热器.根据对水的密度的认识,你估计在阳光照射下水将沿 (填“顺”或“逆”)时针方向流动.

(1)若E1>E2,则该反应为 (填“放热”或“吸热”)反应.该反应可用图 (填“A”或“B”)表示.
(2)若E1<E2,则该反应为 (填“放热”或“吸热”)反应.该反应可用图 (填“A”或“B”)表示.
(3)太阳能的开发和利用是21世纪的一个重要课题.
①利用储能介质储存太阳能的原理是白天在太阳照射下,某种盐熔化,吸收热量;晚间熔盐释放出相应能量,从而使室温得以调节.已知下列数据:
| 盐 | 熔点/℃ | 熔化吸热/KJ?mol-1 | 参考价格/元?kg-1 |
| CaCL2?6H2O | 29,0 | 37,3 | 780~850 |
| Na2SO4?10H2O | 32,4 | 77,0 | 800~900 |
| Na2HPO4?12H2O | 36,1 | 100,1 | 1600~2000 |
| Na2S2O3?5H2O | 48,5 | 49,7 | 1400~1800 |
A.CaCL2?6H2O B、Na2SO4?10H2O C.Na2HPO4?12H2O D、Na2S2O3?5H2O
②右图是一种太阳能热水器的示意图,图中A是集热器,B是储水容器,C是供阴天时加热的辅助电热器.根据对水的密度的认识,你估计在阳光照射下水将沿 (填“顺”或“逆”)时针方向流动.
工业制硫酸中,SO2的催化氧化是一个可逆反应:2SO2+O2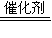 2SO3,即该反应达到一定限度后,就会在反应物和生成物之间建立一种动态平衡(即化学平衡).
2SO3,即该反应达到一定限度后,就会在反应物和生成物之间建立一种动态平衡(即化学平衡).
(1)请填写下表空白:
(2)比较法是一种重要的化学学习方法.请用比较法归纳上表中的反应速率与化学方程式中的计量数之间的关系: .
0 65655 65663 65669 65673 65679 65681 65685 65691 65693 65699 65705 65709 65711 65715 65721 65723 65729 65733 65735 65739 65741 65745 65747 65749 65750 65751 65753 65754 65755 65757 65759 65763 65765 65769 65771 65775 65781 65783 65789 65793 65795 65799 65805 65811 65813 65819 65823 65825 65831 65835 65841 65849 203614
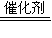 2SO3,即该反应达到一定限度后,就会在反应物和生成物之间建立一种动态平衡(即化学平衡).
2SO3,即该反应达到一定限度后,就会在反应物和生成物之间建立一种动态平衡(即化学平衡).(1)请填写下表空白:
| SO2 | O2 | SO3 | |
| 反应开始时的浓度 /mol?L-1 | 3.0 | 1.5 | |
| 10min后的浓度 /mol?L-1 | |||
| 平均反应速率 /mol?L-1min-1 | 0.1 |