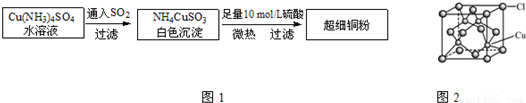
氯化铜晶体是重要的化工原料,可用作催化剂、消毒剂等.用孔雀石[主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物]制备氯化铜晶体,方案如下:
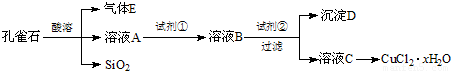
已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:
(1)若溶液A含有的金属离子有Cu2+、Fe2+、Fe3+,则试剂①选用 (填字母).
A.Cu B.Cl2 C.NH3?H2O D.NaOH
(2)加入试剂②的目的是调节pH至a,a的范围是 .由溶液C获得CuCl2?xH2O,包含4个基本实验操作,这4个基本实验操作依次是 、 过滤和无水乙醇洗涤等操作,使用无水乙醇代替水进行洗涤的主要原因是 .
(3)为了测定制得的氯化铜晶体中x值,有同学设计了如下两种实验方案:
①称取一定质量的晶体加热使其失去结晶水,称量所得无水CuCl2的质量.该方案存在的问题是 .
②称取a g晶体、加入足量氢氧化钠溶液,过滤、洗涤、加热沉淀至质量不再减轻为止,称量所得固体的质量为b g.则x= (用含a、b的代数式表示).

已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀的pH | 2.7 | 5.4 | 8.1 |
| 沉淀完全的pH | 3.7 | 6.9 | 9.6 |
A.Cu B.Cl2 C.NH3?H2O D.NaOH
(2)加入试剂②的目的是调节pH至a,a的范围是 .由溶液C获得CuCl2?xH2O,包含4个基本实验操作,这4个基本实验操作依次是 、 过滤和无水乙醇洗涤等操作,使用无水乙醇代替水进行洗涤的主要原因是 .
(3)为了测定制得的氯化铜晶体中x值,有同学设计了如下两种实验方案:
①称取一定质量的晶体加热使其失去结晶水,称量所得无水CuCl2的质量.该方案存在的问题是 .
②称取a g晶体、加入足量氢氧化钠溶液,过滤、洗涤、加热沉淀至质量不再减轻为止,称量所得固体的质量为b g.则x= (用含a、b的代数式表示).
化肥是农业生产最基础而且是最重要的物质投入.工业上利用N2和H2合成氨,其化学方程式为:N2(g)+3H2(g)?2NH3(g)△H<0
(1)下表为不同温度下该反应的平衡常数.由此可推知,表中T1 573K(填“>”、“<”或“=”).
(2)将一定量的N2和H2的混合气放入某密闭容器中发生上述反应.
①下列措施中可提高氢气的转化率的有 (填字母).
A.升高温度 B.使用催化剂
C.增大压强 D.循环利用和不断补充氮气
②在一定温度和压强下,将H2和N2按体积比3:1在密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的体积分数为 ,此时N2的转化率为 .
,此时N2的转化率为 .
(3)某厂每天产生600m3含氨废水.该厂处理废水的方法:将废水加热得到NH3,使废水中NH3的浓度降为17mg?L-1.再对加热蒸发得到的NH3用一定量空气氧化.发生的主反应如下:
4NH3+5O2 4NO+6H2O 4NO+3O2+2H2O=4HNO3
4NO+6H2O 4NO+3O2+2H2O=4HNO3
副反应为:4NH3+3O2=2N2+6H2O
①该厂每天通过加热蒸发可得到NH3的物质的量是多少?
②若氧化过程中90% NH3转化为硝酸,10% NH3发生了副反应,则该厂每天消耗标准状况下的空气多少立方米?(假设废水加热前后的体积和密度近似认为不变,空气中氧气的体积分数20%.)
0 65644 65652 65658 65662 65668 65670 65674 65680 65682 65688 65694 65698 65700 65704 65710 65712 65718 65722 65724 65728 65730 65734 65736 65738 65739 65740 65742 65743 65744 65746 65748 65752 65754 65758 65760 65764 65770 65772 65778 65782 65784 65788 65794 65800 65802 65808 65812 65814 65820 65824 65830 65838 203614
(1)下表为不同温度下该反应的平衡常数.由此可推知,表中T1 573K(填“>”、“<”或“=”).
| T/K | T1 | 573 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
①下列措施中可提高氢气的转化率的有 (填字母).
A.升高温度 B.使用催化剂
C.增大压强 D.循环利用和不断补充氮气
②在一定温度和压强下,将H2和N2按体积比3:1在密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的体积分数为
 ,此时N2的转化率为 .
,此时N2的转化率为 .(3)某厂每天产生600m3含氨废水.该厂处理废水的方法:将废水加热得到NH3,使废水中NH3的浓度降为17mg?L-1.再对加热蒸发得到的NH3用一定量空气氧化.发生的主反应如下:
4NH3+5O2
 4NO+6H2O 4NO+3O2+2H2O=4HNO3
4NO+6H2O 4NO+3O2+2H2O=4HNO3副反应为:4NH3+3O2=2N2+6H2O
①该厂每天通过加热蒸发可得到NH3的物质的量是多少?
②若氧化过程中90% NH3转化为硝酸,10% NH3发生了副反应,则该厂每天消耗标准状况下的空气多少立方米?(假设废水加热前后的体积和密度近似认为不变,空气中氧气的体积分数20%.)
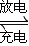 Cd(OH)2+2Ni(OH)2有关该电池的说法正确的是( )
Cd(OH)2+2Ni(OH)2有关该电池的说法正确的是( )