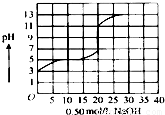
在一定体积的密闭容器中,进行反应CO2(g)+H2(g)?CO(g)+H2O(g).其平衡常数K和温度T的关系如表所示:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=
(2)该反应为 反应(填“吸热”或“放热”)
(3)能判断该反应达化学平衡状态的依据是
A:容器中压强不变 B:混合气体中C(CO)不变
C:V(H2)正=V(H2O)逆D:C(CO2)=C(CO)
(4)某温度下,平衡浓度符合下式:C(CO2)?C(H2)=C(CO)?C(H2O)试判断此时的温度
(5)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为C(CO2) 为2mol/L,C(H2)为1.5mol/L,C(CO) 为1mol/L,C(H2O)为3mol/L,则此时刻反应向 (填“正向”或“逆向”)进行.
| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=
(2)该反应为 反应(填“吸热”或“放热”)
(3)能判断该反应达化学平衡状态的依据是
A:容器中压强不变 B:混合气体中C(CO)不变
C:V(H2)正=V(H2O)逆D:C(CO2)=C(CO)
(4)某温度下,平衡浓度符合下式:C(CO2)?C(H2)=C(CO)?C(H2O)试判断此时的温度
(5)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为C(CO2) 为2mol/L,C(H2)为1.5mol/L,C(CO) 为1mol/L,C(H2O)为3mol/L,则此时刻反应向 (填“正向”或“逆向”)进行.
某学生用0.2000mol?L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:(1)以上步骤有错误的是(填编号) ,该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”) ;
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果(填“偏大”、“偏小”或“无响”) ;
(3)判断滴定终点的现象是:锥形瓶中溶液从 色变为 色,且半分钟不变色;
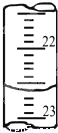
(4)右图是某次滴定时的滴定管中的液面,其读数为 mL;
(5)根据下列数据:请计算待测盐酸溶液的浓度: mol/L.
0 65583 65591 65597 65601 65607 65609 65613 65619 65621 65627 65633 65637 65639 65643 65649 65651 65657 65661 65663 65667 65669 65673 65675 65677 65678 65679 65681 65682 65683 65685 65687 65691 65693 65697 65699 65703 65709 65711 65717 65721 65723 65727 65733 65739 65741 65747 65751 65753 65759 65763 65769 65777 203614
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:(1)以上步骤有错误的是(填编号) ,该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”) ;
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果(填“偏大”、“偏小”或“无响”) ;
(3)判断滴定终点的现象是:锥形瓶中溶液从 色变为 色,且半分钟不变色;
(4)右图是某次滴定时的滴定管中的液面,其读数为 mL;
(5)根据下列数据:请计算待测盐酸溶液的浓度: mol/L.
| 滴定次数 | 待测体积(ml) | 标准烧碱体积(ml) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 4.00 | 24.00 |
| 第三次 | 20.00 | 2.00 | 24.10 |