某学生用0.1×10×25㎜3,质量分数≥99.5%的铝片和酸反应制取H2,实验现象见下表:
(1)写出铝片与酸反应的离子方程式 .
(2)反应1-15min内,铝与盐酸的反应速率逐渐加快,其原因是 .
(3)根据铝片与盐酸和硫酸反应现象的差异,深入思考,可作出如下猜想:
猜想一: ;猜想二: .
0 65546 65554 65560 65564 65570 65572 65576 65582 65584 65590 65596 65600 65602 65606 65612 65614 65620 65624 65626 65630 65632 65636 65638 65640 65641 65642 65644 65645 65646 65648 65650 65654 65656 65660 65662 65666 65672 65674 65680 65684 65686 65690 65696 65702 65704 65710 65714 65716 65722 65726 65732 65740 203614
| 1min | 2min | 5min | 15min | 20min | |
| 3mol/L HCl | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
| 1.5mol/L H2SO4 | 均无明显现象(只有少量气泡) | ||||
(2)反应1-15min内,铝与盐酸的反应速率逐渐加快,其原因是 .
(3)根据铝片与盐酸和硫酸反应现象的差异,深入思考,可作出如下猜想:
猜想一: ;猜想二: .
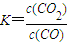 ,已知1100℃时,K=0.263.
,已知1100℃时,K=0.263.