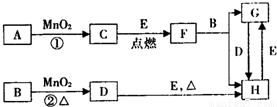
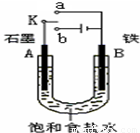
根据表中信息,判断下列叙述中正确的是( )
A.表中①组的反应可能有一种或两种元素被氧化
B.氧化性强弱的比较:KClO3>Fe3+>Cl2>Br2
C.表中②组反应的还原产物是KCl,电子转移数目是6e-
D.表中③组反应的离子方程式为:2MnO4-+3H2O2+6H+=2Mn2++4O2↑+6H2O
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | Cl- | |
| ② | KClO3 | 浓盐酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
A.表中①组的反应可能有一种或两种元素被氧化
B.氧化性强弱的比较:KClO3>Fe3+>Cl2>Br2
C.表中②组反应的还原产物是KCl,电子转移数目是6e-
D.表中③组反应的离子方程式为:2MnO4-+3H2O2+6H+=2Mn2++4O2↑+6H2O
下列实验“操作和现象”与“结论”都正确的是( )
A.A
B.B
C.C
D.D
| 操作和现象 | 结论 | |
| A | 切开金属钠,钠表面的银白色会逐渐褪去 | Na在空气中会生成Na2O2 |
| B | 铝箔插入浓硝酸中,无明显现象 | 铝与浓硝酸不反应 |
| C | SO2通入酸性KMnO4溶液,溶液褪色 | SO2具有漂白性 |
| D | 将充满NO2的试管倒立在水中,试管内液面约上升至试管容积的 处;缓慢通入O2,轻轻晃动试管,至液体基本上充满试管 处;缓慢通入O2,轻轻晃动试管,至液体基本上充满试管 | 从原料的充分利用和减少污染物的排放等方面考虑,该实验对工业生产硝酸有重要启示 |
A.A
B.B
C.C
D.D
下列实验中,依据实验操作及现象,得出的结论正确的是( )
A.A
B.B
C.C
D.D
| 操作 | 现象 | 结论 | |
| A | 用CH3COOH溶液浸泡水垢 | 水垢溶解,有无色气泡 | 碱性:NaHCO3>CH3COONa |
B | 测定等浓度的Na2CO3和Na2SO3溶液的pH | 前者pH比后者的大 | 非金属性:S>C |
| C | 向FeBr2溶液中通入过量Cl2 | 溶液由浅绿色变成黄色 | 氧化性:Br2>Fe3+ |
| D | 向盛有1mL 0.1mol?L-1 AgNO3溶液的试管中滴加2~4滴0.1mol?L-1 NaCl溶液,后继续滴加 0.1mol?L-1 KI溶液. | 出现黄色沉淀 | 溶解度:AgCl>AgI |
A.A
B.B
C.C
D.D
图甲为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
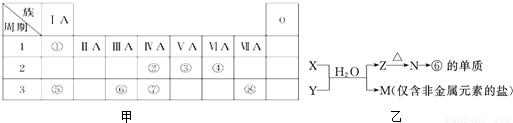
(1)②、⑦的最高价含氧酸的酸性是由强到弱的,用原子结构解释原因:______,原子半径逐渐增大,得电子能力逐渐减弱,非金属性逐渐减弱.
(2)以上元素可形成多种化合物,其中既含离子键又含非极性共价键的化合物的电子式为______.
(3)W与④是相邻的同主族元素.在下表中列出H2WO3的各种不同化学性质,举例并写出相应的化学方程式.
(4)由图甲中元素形成的常见物质X、Y、Z、M、N可发生图乙所示反应:
X溶液与Y溶液反应的离子方程式______;
N→⑥的单质的化学方程式为______电解4Al+3O2↑

(1)②、⑦的最高价含氧酸的酸性是由强到弱的,用原子结构解释原因:______,原子半径逐渐增大,得电子能力逐渐减弱,非金属性逐渐减弱.
(2)以上元素可形成多种化合物,其中既含离子键又含非极性共价键的化合物的电子式为______.
(3)W与④是相邻的同主族元素.在下表中列出H2WO3的各种不同化学性质,举例并写出相应的化学方程式.
| 编号 | 性质 | 化学方程式 |
| 示例 | 氧化性 | H2WO3+3H3PO3═3H3PO4+H2W↑ |
| 1 | ______ | ______ |
| 2 | ______ | ______ |
X溶液与Y溶液反应的离子方程式______;
N→⑥的单质的化学方程式为______电解4Al+3O2↑
海水资源的利用具有广阔前景.海水中主要离子的含量如下:
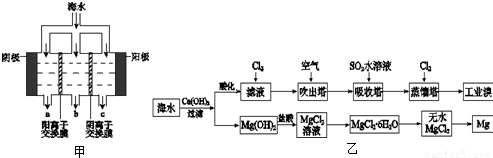
(1)电渗析法淡化海水示意图如图甲所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过.
①阳极主要电极反应式是______.
②在阴极附近产生少量白色沉淀,其成分有______和CaCO3,生成CaCO3的离子方程式是______.
③淡水的出口为______(填“a”、“b”或“c”).
(2)利用海水可以提取溴和镁,提取过程如图乙所示:
①提取溴的过程中,经过2次Br-→Br2转化的目的是______,吸收塔中发生反应的离子方程式是______.解释通空气的目的是______.
②从MgCl2溶液中得到MgCl2?6H2O晶体的主要操作是______、过滤、洗涤、干燥.
③依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为______L(忽略Cl2溶解).
0 65022 65030 65036 65040 65046 65048 65052 65058 65060 65066 65072 65076 65078 65082 65088 65090 65096 65100 65102 65106 65108 65112 65114 65116 65117 65118 65120 65121 65122 65124 65126 65130 65132 65136 65138 65142 65148 65150 65156 65160 65162 65166 65172 65178 65180 65186 65190 65192 65198 65202 65208 65216 203614
| 成分 | 含量/(mg L-1) | 成分 | 含量/(mg L-1) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42 | 2560 | Br- | 64 |
| Mg2+ | 1272 |

(1)电渗析法淡化海水示意图如图甲所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过.
①阳极主要电极反应式是______.
②在阴极附近产生少量白色沉淀,其成分有______和CaCO3,生成CaCO3的离子方程式是______.
③淡水的出口为______(填“a”、“b”或“c”).
(2)利用海水可以提取溴和镁,提取过程如图乙所示:
①提取溴的过程中,经过2次Br-→Br2转化的目的是______,吸收塔中发生反应的离子方程式是______.解释通空气的目的是______.
②从MgCl2溶液中得到MgCl2?6H2O晶体的主要操作是______、过滤、洗涤、干燥.
③依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为______L(忽略Cl2溶解).