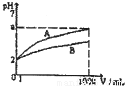
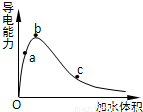
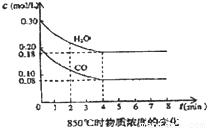
在一体积为10L的容器中,通入一定量的CO和H2O,在85℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-Q kJ/mol CO和H2O浓度变化如图,则
(1)0-4min的平均反应速率v(CO)= mol/
(2)下列能说明反应达到平衡状态的是 .
a、每消耗1mol CO2的同时生成l molH2O b、体系压强保持不变
c、v正(CO)=v逆(CO2) d、容器中混合气体的密度保持不变
e、混合气体中H2O的体积分数保持不变 f、CO2和H2的体积比保持不变
t1℃时物质浓度(mol/L)的变化
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表.
①表中3min-4min之间反应处于 状态;C1数值 0.08mol/L(填大于、小于或等于).
②反应在4min-5min之间,平衡向逆方向移动,可能的原因是 (单选),表中5min-6min之间数值发生变化,可能的原因是 (单选).
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度.
(1)0-4min的平均反应速率v(CO)= mol/
(2)下列能说明反应达到平衡状态的是 .
a、每消耗1mol CO2的同时生成l molH2O b、体系压强保持不变
c、v正(CO)=v逆(CO2) d、容器中混合气体的密度保持不变
e、混合气体中H2O的体积分数保持不变 f、CO2和H2的体积比保持不变
t1℃时物质浓度(mol/L)的变化
| 时间 | CO | H2O | CO2 | H2 |
| 0.200 | 0.300 | |||
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
①表中3min-4min之间反应处于 状态;C1数值 0.08mol/L(填大于、小于或等于).
②反应在4min-5min之间,平衡向逆方向移动,可能的原因是 (单选),表中5min-6min之间数值发生变化,可能的原因是 (单选).
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度.

工业合成氨与制备硝酸一般可连续生产,流程如下

(1)①工业生产时,制取氢气的一个反应为:CO+H2O(g)?CO2+H2,850℃时,往1L密闭容器中充入0.3mol CO和0.2molH2O(g).反应4min后建立平衡,体系中c(H2)=0.12mol?L-1.CO的平衡浓度为 转化率为 该温度下此反应的平衡常数K= (填计算结果).
②在850℃时,以表中的物质的量投入恒容反应器中,其中向逆反应方向进行的有 (选填A、B、C、D、E)
(2)合成塔中发生反应N2(g)+3H2(g)?2NH3(g)△H<0.下表为不同温度下该反应的平衡常数.由此可推知,表中T1 300℃(填“>”、“<”或“=”).
(3)N2和H2在铁作催化剂作用下从145℃就开始反应,不同温度下NH3产率图1所示.温度高于900℃时,NH3产率下降,原因是 .
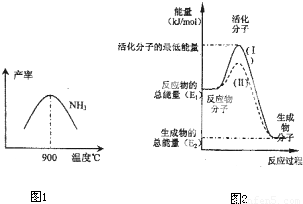
(4)在化学反应中只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ?mol-1表示.请认真观察图2,回答问题.
图中所示反应是 (填“吸热”或“放热”)反应,该反应的△H= (用含E1、E2E的代数式表示).已知热化学方程式:H2(g)+ O2(g)=H2O(g)△H=-241.8kJ?mol-1,该反应的活化能为167.2kJ?mol-1,则其逆反应的活化能为 .
O2(g)=H2O(g)△H=-241.8kJ?mol-1,该反应的活化能为167.2kJ?mol-1,则其逆反应的活化能为 .
(5)硝酸厂的尾气直接排放将污染空气.目前科学家探索利用燃料气体中的甲烷等将氮的氧化物还原为氮气和水,反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ?mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ?mol-1
则甲烷直接将NO2还原为N2的热化学方程式为: .
0 64711 64719 64725 64729 64735 64737 64741 64747 64749 64755 64761 64765 64767 64771 64777 64779 64785 64789 64791 64795 64797 64801 64803 64805 64806 64807 64809 64810 64811 64813 64815 64819 64821 64825 64827 64831 64837 64839 64845 64849 64851 64855 64861 64867 64869 64875 64879 64881 64887 64891 64897 64905 203614

(1)①工业生产时,制取氢气的一个反应为:CO+H2O(g)?CO2+H2,850℃时,往1L密闭容器中充入0.3mol CO和0.2molH2O(g).反应4min后建立平衡,体系中c(H2)=0.12mol?L-1.CO的平衡浓度为 转化率为 该温度下此反应的平衡常数K= (填计算结果).
②在850℃时,以表中的物质的量投入恒容反应器中,其中向逆反应方向进行的有 (选填A、B、C、D、E)
| A | B | C | D | E | |
| n(CO2) | 3 | l | 1 | l | |
| n(H2) | 2 | l | 1 | 2 | |
| n(CO) | 1 | 2 | 3 | 0.5 | 3 |
| n(H2O) | 5 | 2 | 3 | 2 | l |
| T/°C | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |

(4)在化学反应中只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ?mol-1表示.请认真观察图2,回答问题.
图中所示反应是 (填“吸热”或“放热”)反应,该反应的△H= (用含E1、E2E的代数式表示).已知热化学方程式:H2(g)+
 O2(g)=H2O(g)△H=-241.8kJ?mol-1,该反应的活化能为167.2kJ?mol-1,则其逆反应的活化能为 .
O2(g)=H2O(g)△H=-241.8kJ?mol-1,该反应的活化能为167.2kJ?mol-1,则其逆反应的活化能为 .(5)硝酸厂的尾气直接排放将污染空气.目前科学家探索利用燃料气体中的甲烷等将氮的氧化物还原为氮气和水,反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ?mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ?mol-1
则甲烷直接将NO2还原为N2的热化学方程式为: .