室温下,将1.00mol/L盐酸滴入20.00mL 1.00mol/L氨水中,溶液pH和温度(℃)
随加入盐酸体积变化曲线如图所示.
(1)下列有关说法正确的是______
A.a点由水电离出的c(H+)=10-14mol/L
B.b点:c(NH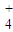 )+c=c(Cl-)
)+c=c(Cl-)
C.c点:C(Cl-)=C(NH4+)
D.d点后,溶液温度略下降的主要原因是NH3?H2O电离吸热
(2)在滴加过程中,水的电离程度的变化是先______后______(填“增大”、“减小”或“不变”);
(3)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序,对应溶质的化学式和溶液的pH.试填写表中空白:
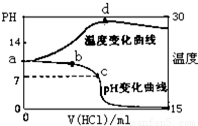
随加入盐酸体积变化曲线如图所示.
(1)下列有关说法正确的是______
A.a点由水电离出的c(H+)=10-14mol/L
B.b点:c(NH
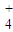 )+c=c(Cl-)
)+c=c(Cl-)C.c点:C(Cl-)=C(NH4+)
D.d点后,溶液温度略下降的主要原因是NH3?H2O电离吸热
(2)在滴加过程中,水的电离程度的变化是先______后______(填“增大”、“减小”或“不变”);
(3)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序,对应溶质的化学式和溶液的pH.试填写表中空白:
| 离子浓度的关系 | 溶质 | 溶液的pH | 物料守恒关系 | |
| ① | C(NH4+)>C(Cl-)>C(OH-)>C(H+) | ______ | pH>7 | / |
| ② | NH4Cl | / | ______ | |
| ③ | C(Cl-)>C(H+)>C(NH4+)>C(OH-) | ______ | pH<7 | / |

某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂.请填写下列空白:
(1)终点的判断:溶液由______.
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是______
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
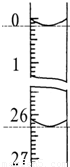
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为______ml.
(4)某学生根据3次实验分别记录有关数据如表:
②依据上表数据计算该NaOH溶液的物质的量浓度______ (计算结果取4位有效数).
0 64605 64613 64619 64623 64629 64631 64635 64641 64643 64649 64655 64659 64661 64665 64671 64673 64679 64683 64685 64689 64691 64695 64697 64699 64700 64701 64703 64704 64705 64707 64709 64713 64715 64719 64721 64725 64731 64733 64739 64743 64745 64749 64755 64761 64763 64769 64773 64775 64781 64785 64791 64799 203614
(1)终点的判断:溶液由______.
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是______
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为______ml.
(4)某学生根据3次实验分别记录有关数据如表:
| 滴定 次数 | 待测NaOH溶液的体积/mL | 0.1000mol/L盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 平均耗用盐酸 体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.15 | ①V=______ |
| 第二次 | 25.00 | 0.56 | 30.30 | |
| 第三次 | 25.00 | 0.20 | 26.35 | |