根据表1信息,判断以下叙述正确的是:( )
表1 部分短周期元素的原子半径及主要化合价
A.氢化物的沸点为H2T<H2R
B.M与T形成的化合物具有两性
C.单质与稀盐酸反应的剧烈程度为L<Q
D.L2+与R2-的核外电子数相等
表1 部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.氢化物的沸点为H2T<H2R
B.M与T形成的化合物具有两性
C.单质与稀盐酸反应的剧烈程度为L<Q
D.L2+与R2-的核外电子数相等
下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质 的是:
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是 ,碱性最强的化合物的是: .
(3)最高价氧化物是两性氧化物的元素是 ;写出它的氢氧化物与氢氧化钠反应的离子方程式 .
(4)用电子式表示元素④与⑥的化合物的形成过程: ,该化合物属于 (填“共价”或“离子”)化合物.
(5)表示①与③的化合物的电子式 ,该化合物是由 (填“极性”“非极性”下同)键形成的.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是 ,碱性最强的化合物的是: .
(3)最高价氧化物是两性氧化物的元素是 ;写出它的氢氧化物与氢氧化钠反应的离子方程式 .
(4)用电子式表示元素④与⑥的化合物的形成过程: ,该化合物属于 (填“共价”或“离子”)化合物.
(5)表示①与③的化合物的电子式 ,该化合物是由 (填“极性”“非极性”下同)键形成的.
下表中的数据是破坏1mol物质中的化学键所吸收的能量(kJ).这一数据的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热,反应热等于反应中断裂旧化学键消耗的能量之和与反应中形成新化学键放出的能量之和的差.回答下列问题:
(1)在HCl、HBr、HI中,最稳定的是 ;
(2)对于反应X2+H2=2HX(X2代表Cl2、Br2、I2),相同条件下,消耗等量氢气时,放出热量最多的是 ;
(3)反应Br2+H2=2HBr,当生成2mol HBr时放出 kJ能量.
0 64396 64404 64410 64414 64420 64422 64426 64432 64434 64440 64446 64450 64452 64456 64462 64464 64470 64474 64476 64480 64482 64486 64488 64490 64491 64492 64494 64495 64496 64498 64500 64504 64506 64510 64512 64516 64522 64524 64530 64534 64536 64540 64546 64552 64554 64560 64564 64566 64572 64576 64582 64590 203614
| 化学键 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
(2)对于反应X2+H2=2HX(X2代表Cl2、Br2、I2),相同条件下,消耗等量氢气时,放出热量最多的是 ;
(3)反应Br2+H2=2HBr,当生成2mol HBr时放出 kJ能量.
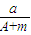 (A-N+m)mol
(A-N+m)mol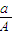 (A-N)mol
(A-N)mol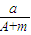 (A-N)mol
(A-N)mol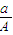 (A-N+m)mol
(A-N+m)mol