某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净,待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入20.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净,再用标准酸液润洗2-3次后,向其中注入0.1000mol?L-1标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL.
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.
试回答下列问题:
(1)锥形瓶中的溶液从______色变为______ 色时,停止滴定.
(2)该小组在步骤①中的错误是______,由此造成的测定结果______(偏高、偏低或无影响).
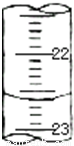
(3)如图,是某次滴定时的滴定管中的液面,其读数为______mL.
(4)根据下列数据:
请计算待测烧碱溶液的浓度为______ mol?L-1.
①将碱式滴定管用蒸馏水洗净,待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入20.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净,再用标准酸液润洗2-3次后,向其中注入0.1000mol?L-1标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL.
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.
试回答下列问题:
(1)锥形瓶中的溶液从______色变为______ 色时,停止滴定.
(2)该小组在步骤①中的错误是______,由此造成的测定结果______(偏高、偏低或无影响).
(3)如图,是某次滴定时的滴定管中的液面,其读数为______mL.
(4)根据下列数据:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.50 | 25.40 |
| 第二次 | 20.00 | 4.00 | 29.10 |

( I)在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的交化如下表:
(1)写出该反应的平衡常数表达式:K=______,已知:K(300℃)>K(350℃),该反应是______反应(填“放热”或“吸热”);
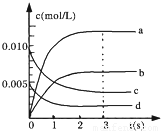
(2)如图中表示NO2的变化的曲线是______,用O2的浓度变化表示从0~2s内该反应的平均速率v=______;
(3)能说明该反应已经达到平衡状态的是______
a. v(NO2)=2v(O2);b.容器内压强保持不变;c.v逆(NO)=2v正(O2);d.容器内物质的密度保持不变.
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是______
a.及时分离出NO2气体;b.适当升高温度;c.增大O2的浓度;d.选择高效的催化剂.
( II)用石墨做电极电解:①稀H2SO4 ②K2SO4溶液 ③CuCl2溶液 ④CuSO4 溶液 ⑤KOH溶液.
(1)阴阳极都有气体产生,且体积比(相同条件下)为2:1的是______(填序号,下同),其阳极的电极反应式都是______,总反应的化学方程式是______ 2H2↑+O2↑
0 64106 64114 64120 64124 64130 64132 64136 64142 64144 64150 64156 64160 64162 64166 64172 64174 64180 64184 64186 64190 64192 64196 64198 64200 64201 64202 64204 64205 64206 64208 64210 64214 64216 64220 64222 64226 64232 64234 64240 64244 64246 64250 64256 64262 64264 64270 64274 64276 64282 64286 64292 64300 203614
| 时间/s | 1 | 2 | 3 | 4 | 5 | |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图中表示NO2的变化的曲线是______,用O2的浓度变化表示从0~2s内该反应的平均速率v=______;
(3)能说明该反应已经达到平衡状态的是______
a. v(NO2)=2v(O2);b.容器内压强保持不变;c.v逆(NO)=2v正(O2);d.容器内物质的密度保持不变.
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是______
a.及时分离出NO2气体;b.适当升高温度;c.增大O2的浓度;d.选择高效的催化剂.
( II)用石墨做电极电解:①稀H2SO4 ②K2SO4溶液 ③CuCl2溶液 ④CuSO4 溶液 ⑤KOH溶液.
(1)阴阳极都有气体产生,且体积比(相同条件下)为2:1的是______(填序号,下同),其阳极的电极反应式都是______,总反应的化学方程式是______ 2H2↑+O2↑

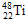 、
、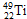 、中,中子数不可能为( )
、中,中子数不可能为( )