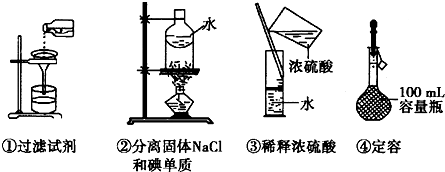
完成下列实验所选择的装置或仪器 (夹持装置己略去)正确的是
| A | B | C | D | |
| 实验 | 用CCl4提取碘水中的I2 | 分离乙醇中的I2 | 加热分解 MgCl26H2O得到 纯净的MgCl2 | 配制100mL 10.1000mol/L K2Cr2O7溶液 |
| 装置或仪器 |  | 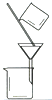 | 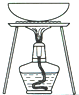 | 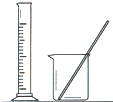 |
- A.A
- B.B
- C.C
- D.D
 (1)1.2g RSO4中含0.01mol R2+,则RSO4的摩尔质量是______;R的相对原子质量约是______.
(1)1.2g RSO4中含0.01mol R2+,则RSO4的摩尔质量是______;R的相对原子质量约是______.
(2)病人输液用的葡萄糖注射液是葡萄糖(化学式为C6H12O6)的水溶液,其标签上的部分内容如图所示.利用标签所提供的信息,回答下列问题:
①该注射液中葡萄糖的质量分数为______;
②该注射液中葡萄糖的物质的量浓度为______.
(3)现有一瓶A和B的混合液,已知它们的性质如下表.
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g?cm-3 | 溶解性 |
| A | -11.5 | 198 | 1.11 | A、B互溶,且均易溶于水 |
| B | 17.9 | 290 | 1.26 |
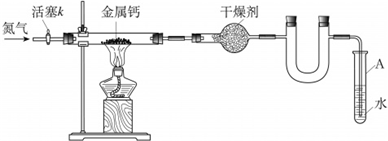
 氮的化合物在某些领域中扮演着重要的角色.
氮的化合物在某些领域中扮演着重要的角色.