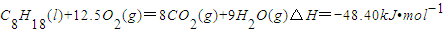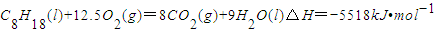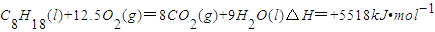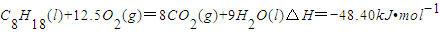用中和滴定法测定烧碱的纯度,已知烧碱中杂质不与酸反应,试根据要求填空:
(1)配置待测液:称取5.0g烧碱样品,配成250mL待测溶液;
(2)滴定:用0.2000mol?L-1标准盐酸溶液滴定待测溶液,下面的操作错误的有 .
①用标准盐酸溶液润洗酸式滴定管;
②用待测烧碱溶液润洗锥形瓶;
③两个同学合作,一人控制酸式滴定管的活塞,另一人摇动锥形瓶;
④滴定过程中,操作者的眼睛始终注视酸式滴定管液面的变化.
(3)根据下表数据计算:①待测烧碱溶液的物质的量浓度: (结果保留4位有效字);
②烧碱的纯度: .
(1)配置待测液:称取5.0g烧碱样品,配成250mL待测溶液;
(2)滴定:用0.2000mol?L-1标准盐酸溶液滴定待测溶液,下面的操作错误的有 .
①用标准盐酸溶液润洗酸式滴定管;
②用待测烧碱溶液润洗锥形瓶;
③两个同学合作,一人控制酸式滴定管的活塞,另一人摇动锥形瓶;
④滴定过程中,操作者的眼睛始终注视酸式滴定管液面的变化.
(3)根据下表数据计算:①待测烧碱溶液的物质的量浓度: (结果保留4位有效字);
②烧碱的纯度: .
| 滴定次数 | 待测溶液 体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.45 |
| 第二次 | 10.00 | 4.00 | 24.05 |
在80℃时,将0.40mol的N2O4气体充入1L固定容积的密闭容器中发生反应:N2O4═2NO2(△H>0),每隔一段时间对容器内的物质进行测定,得到如下数据:
(1)在20s-40s之间,用N2O4表示的平均反应速率为 .
(2)在80℃时该反应的平衡常数K= .
(3)要增大该反应的平衡常数,可采取的措施有(填序号) .
①增大N2O4的起始浓度 ②向混合气体中通入NO2
③使用高效催化剂 ④升高温度
(4)反应进行至100s后若降低温度,混合气体的颜色 (填“变浅”、“变深”或“不变”).
(5)反应进行至100s后若向容器中再充入0.40mol的N2O4气体,则达到新平衡后N2O4的转化率将 (填“增大”、“减小”或“不变”).
| 时间(s) | 20 | 40 | 60 | 80 | 100 | |
| n(N2O4)(mol) | 0.40 | a | 0.20 | c | d | e |
| n(NO2)(mol) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(2)在80℃时该反应的平衡常数K= .
(3)要增大该反应的平衡常数,可采取的措施有(填序号) .
①增大N2O4的起始浓度 ②向混合气体中通入NO2
③使用高效催化剂 ④升高温度
(4)反应进行至100s后若降低温度,混合气体的颜色 (填“变浅”、“变深”或“不变”).
(5)反应进行至100s后若向容器中再充入0.40mol的N2O4气体,则达到新平衡后N2O4的转化率将 (填“增大”、“减小”或“不变”).
Br2和Fe3+的水溶液浓度较小时均呈现黄色,二者都具有较强的氧化性.某化学兴趣小组拟通过探究实验来比较二者氧化性的强弱.
实验操作:向足量的硫酸亚铁溶液中加入少量浓溴水,振荡.
实验现象:溶液由浅绿色变为黄色.
(1)提出假设:
甲同学认为氧化性:Br2>Fe3+,则反应的离子方程式为______;
乙同学认为氧化性:Fe3+>Br2,则使溶液呈黄色的物质是______(填化学式).
(2)通过进一步实验可以检验甲和乙的结论谁对谁错,下列是设计的一些实验方案和预测:
①方案1是否合理______(填“是”或“否”).
②方案2中,由于存在反应______(用离子方程式表示),所以预测结论不正确.
③请另外设计一个合理方案,证明已经发生反应.将有关内容填入下表.
实验操作:向足量的硫酸亚铁溶液中加入少量浓溴水,振荡.
实验现象:溶液由浅绿色变为黄色.
(1)提出假设:
甲同学认为氧化性:Br2>Fe3+,则反应的离子方程式为______;
乙同学认为氧化性:Fe3+>Br2,则使溶液呈黄色的物质是______(填化学式).
(2)通过进一步实验可以检验甲和乙的结论谁对谁错,下列是设计的一些实验方案和预测:
| 方案 | 实验操作 | 预期现象及结论 |
| 1 | 取少量黄色溶液,加入NaOH溶液 | 若生成红褐色沉淀,则甲正确 |
| 2 | 取少量黄色溶液,加入淀粉KI溶液 | 若溶液变蓝色,则乙正确 |
| 3 | 取少量黄色溶液,加入苯溶液,振荡后静置 | 若上层溶液呈橙红色,则______正确 |
②方案2中,由于存在反应______(用离子方程式表示),所以预测结论不正确.
③请另外设计一个合理方案,证明已经发生反应.将有关内容填入下表.
| 实验操作 | 预期现象及结论 |
| ______ | ______ |
已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g),△H=-1025kJ/mol,该反应是一个可逆反应,若反应物起始的物质的量相同,下列关于该反应的示意图不正确的是( )
A.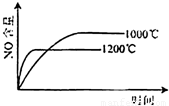
B.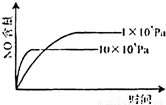
C.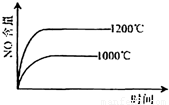
D.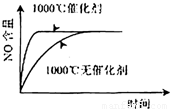
0 63095 63103 63109 63113 63119 63121 63125 63131 63133 63139 63145 63149 63151 63155 63161 63163 63169 63173 63175 63179 63181 63185 63187 63189 63190 63191 63193 63194 63195 63197 63199 63203 63205 63209 63211 63215 63221 63223 63229 63233 63235 63239 63245 63251 63253 63259 63263 63265 63271 63275 63281 63289 203614
A.

B.

C.

D.