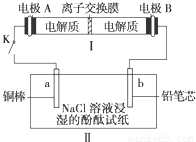
下列实验中,依据实验操作及现象,得出的结论正确的是( )
A.A
B.B
C.C
D.D
| 操作 | 现象 | 结论 | |
| A | 用CH3COOH溶液浸泡水垢 | 水垢溶解,有无色气泡 | 碱性:NaHCO3>CH3COONa |
B | 测定等浓度的Na2CO3和Na2SO3溶液的pH | 前者pH比后者的大 | 非金属性:S>C |
| C | 向FeBr2溶液中通入过量Cl2 | 溶液由浅绿色变成黄色 | 氧化性:Br2>Fe3+ |
| D | 向盛有1mL 0.1mol?L-1 AgNO3溶液的试管中滴加2~4滴0.1mol?L-1 NaCl溶液,后继续滴加 0.1mol?L-1 KI溶液. | 出现黄色沉淀 | 溶解度:AgCl>AgI |
A.A
B.B
C.C
D.D
复分解反应存在这样一个规律:较强酸可制取较弱酸.中和反应、盐类的水解也是复分解反应,盐类的水解反应的逆反应是中和反应.盐类的水解反应中,弱酸强碱盐中弱酸根离子对应的弱酸越弱,其盐越容易发生水解.
已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH:
(1)请根据上述信息判断下列反应不能发生的是______(填编号).
A.CO2+H2O+2NaClO═Na2CO3+2HClO
B.CO2+H2O+NaClO═NaHCO3+HClO
C.CO2+H2O+C6H5ONa-→NaHCO3+C6H5OH
D.CO2+H2O+2C6H5ONa-→Na2CO3+2C6H5OH
E.Na2CO3+C6H5OH-→NaHCO3+C6H5ONa
F.CH3COOH+NaCN═CH3COONa+HCN
(2)一些复分解反应的发生还遵循其他的规律.下列变化都属于复分解反应:
①将石灰乳与纯碱溶液混合可制得苛性钠溶液
②向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打固体
③蒸发KCl和NaNO3的混合溶液,首先析出NaCl晶体.
根据上述反应,总结出复分解反应发生的另一规律为______.
(3)物质的量浓度均为0.05mol/L的下列五种物质的溶液中,pH由大到小的顺序是______(填编号).
①C6H5OH(苯酚) ②CH3COOH ③HClO4 ④HClO ⑤H2SO4
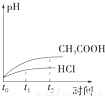
(4)一定温度下,向等体积纯水中分别加入等物质的量的下列物质:①NaOH、②CH3COOH、③NaClO,则水的电离程度最大的是______(填编号).
(5)25℃时,M酸溶液的pH=a,N碱溶液的pH=b.
①若X为强酸,Y为强碱,且a+b=14,若两者等体积混合后,溶液的pH=______,此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是______.
②若X的化学式为HR,Y的化学式为MOH,且a+b=14,两者等体积混合后溶液显酸性,则混合溶液中必定有一种离子能发生水解,该离子为______(填离子符号);混合后的溶液中,下列微粒浓度大小关系正确的是______(填序号).
a c(MOH)>c(M+)>c(R-)>c(H+)>c(OH-)
b c(HR)>c(M+)>c(R-)>c(OH-)>c(H+)
c c(R-)>c(M+)>c(H+)>c(OH-)
d c(M+)>c(R-)>c(OH-)>c(H+)
e c(M+)+c(H+)=c(R-)+c(OH-)
已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 8.1 | 11.6 | 10.3 | 11.1 | 11.3 |
A.CO2+H2O+2NaClO═Na2CO3+2HClO
B.CO2+H2O+NaClO═NaHCO3+HClO
C.CO2+H2O+C6H5ONa-→NaHCO3+C6H5OH
D.CO2+H2O+2C6H5ONa-→Na2CO3+2C6H5OH
E.Na2CO3+C6H5OH-→NaHCO3+C6H5ONa
F.CH3COOH+NaCN═CH3COONa+HCN
(2)一些复分解反应的发生还遵循其他的规律.下列变化都属于复分解反应:
①将石灰乳与纯碱溶液混合可制得苛性钠溶液
②向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打固体
③蒸发KCl和NaNO3的混合溶液,首先析出NaCl晶体.
根据上述反应,总结出复分解反应发生的另一规律为______.
(3)物质的量浓度均为0.05mol/L的下列五种物质的溶液中,pH由大到小的顺序是______(填编号).
①C6H5OH(苯酚) ②CH3COOH ③HClO4 ④HClO ⑤H2SO4
(4)一定温度下,向等体积纯水中分别加入等物质的量的下列物质:①NaOH、②CH3COOH、③NaClO,则水的电离程度最大的是______(填编号).
(5)25℃时,M酸溶液的pH=a,N碱溶液的pH=b.
①若X为强酸,Y为强碱,且a+b=14,若两者等体积混合后,溶液的pH=______,此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是______.
②若X的化学式为HR,Y的化学式为MOH,且a+b=14,两者等体积混合后溶液显酸性,则混合溶液中必定有一种离子能发生水解,该离子为______(填离子符号);混合后的溶液中,下列微粒浓度大小关系正确的是______(填序号).
a c(MOH)>c(M+)>c(R-)>c(H+)>c(OH-)
b c(HR)>c(M+)>c(R-)>c(OH-)>c(H+)
c c(R-)>c(M+)>c(H+)>c(OH-)
d c(M+)>c(R-)>c(OH-)>c(H+)
e c(M+)+c(H+)=c(R-)+c(OH-)
T、X、Y、Z、Q、R、P、W为周期表前四周期元素,原子序数依次递增,其相关信息如表:
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是______(用元素符号表示,下同).
(2)T、X两种元素组成的一种化合物M是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,则M分子中σ键和π键的个数比为______.
(3)将amolQ单质与bmolR单质组成的固体混合物投入到足量的水中,若固体完全溶解最终得到澄清溶液,则同时产生的气体的物质的量为______mol(用a、b表示);当a=b时,写出反应的离子方程式______.
(4)Y2T4分子中Y原子轨道的杂化类型为______.Y2T4用亚硝酸氧化可生成另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977.写出Y2T4与亚硝酸反应的化学方程式______;
(5)YT3的沸点比化合物XT4的高,其主要原因是:______;
(6)P的单质与T、Z形成的既有极性化学键又有非极性化学键共价化合物反应的离子方程式为______.
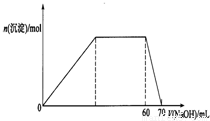
(7)上述八种元素形成的微粒中的两种可与硫酸根形成一种复盐,向该盐的浓溶液中逐滴加入0.1mol/L氢氧化钠溶液,随着氢氧化钠溶液的加入,产生沉淀的关系如图,则该复盐的化学式为______.
0 63049 63057 63063 63067 63073 63075 63079 63085 63087 63093 63099 63103 63105 63109 63115 63117 63123 63127 63129 63133 63135 63139 63141 63143 63144 63145 63147 63148 63149 63151 63153 63157 63159 63163 63165 63169 63175 63177 63183 63187 63189 63193 63199 63205 63207 63213 63217 63219 63225 63229 63235 63243 203614
| 元素 | 相 关 信 息 |
| T | T原子所处的周期数、族序数分别与其原子序数相等 |
| X | X的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同 |
| Z | Z可形成Z2、Z3两种气态单质 |
| Q | 在该元素所在周期中,Q的基态原子的第一电离能最小 |
| R | R的离子为单核离子,且离子半径是与其具有相同电子层结构离子中半径最小的 |
| P | Z是P不同周期的邻族元素;R和P的原子序数之和为30 |
| W | W的一种核素的质量数为56,中子数为30 |
(2)T、X两种元素组成的一种化合物M是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,则M分子中σ键和π键的个数比为______.
(3)将amolQ单质与bmolR单质组成的固体混合物投入到足量的水中,若固体完全溶解最终得到澄清溶液,则同时产生的气体的物质的量为______mol(用a、b表示);当a=b时,写出反应的离子方程式______.
(4)Y2T4分子中Y原子轨道的杂化类型为______.Y2T4用亚硝酸氧化可生成另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977.写出Y2T4与亚硝酸反应的化学方程式______;
(5)YT3的沸点比化合物XT4的高,其主要原因是:______;
(6)P的单质与T、Z形成的既有极性化学键又有非极性化学键共价化合物反应的离子方程式为______.
(7)上述八种元素形成的微粒中的两种可与硫酸根形成一种复盐,向该盐的浓溶液中逐滴加入0.1mol/L氢氧化钠溶液,随着氢氧化钠溶液的加入,产生沉淀的关系如图,则该复盐的化学式为______.





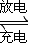 Na2S4+3NaBr.闭合开关K时,b极附近先变红色.下列说法正确的是( )
Na2S4+3NaBr.闭合开关K时,b极附近先变红色.下列说法正确的是( )