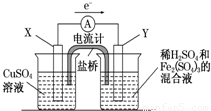
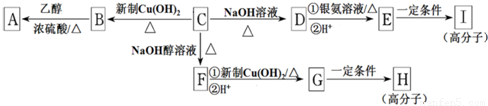
根据表中信息,判断下列叙述中正确的是( )
A.表中①组的反应可能有一种或两种元素被氧化
B.氧化性强弱的比较:KClO3>Fe3+>Cl2>Br2
C.表中②组反应的还原产物是KCl,电子转移数目是6e-
D.表中③组反应的离子方程式为:2MnO4-+3H2O2+6H+=2Mn2++4O2↑+6H2O
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | Cl- | |
| ② | KClO3 | 浓盐酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
A.表中①组的反应可能有一种或两种元素被氧化
B.氧化性强弱的比较:KClO3>Fe3+>Cl2>Br2
C.表中②组反应的还原产物是KCl,电子转移数目是6e-
D.表中③组反应的离子方程式为:2MnO4-+3H2O2+6H+=2Mn2++4O2↑+6H2O
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题: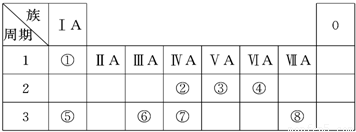
(1)地壳中含量居于第二位的元素在周期表中的位置是______.
(2)②、⑦的最高价含氧酸的酸性是由强到弱的,用原子结构解释原因:______,原子半径逐渐增大,得电子能力逐渐减弱,非金属性逐渐减弱.
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含共价键的离子化合物,写出其中一种化合物的电子式______.
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,下列物质不能做该反应催化剂的是(填序号)______.
a.MnO2 b.CuSO4 c.Na2SO3 d.FeCl3
(5)W与④是相邻的同主族元素.在下表中列出H2WO3的各种不同化学性质,举例并写出相应的化学方程式.
(6)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应(如图):
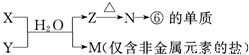
X溶液与Y溶液反应的离子方程式______,
N→⑥的单质的化学方程式为______冰晶石4Al+3O2↑

(1)地壳中含量居于第二位的元素在周期表中的位置是______.
(2)②、⑦的最高价含氧酸的酸性是由强到弱的,用原子结构解释原因:______,原子半径逐渐增大,得电子能力逐渐减弱,非金属性逐渐减弱.
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含共价键的离子化合物,写出其中一种化合物的电子式______.
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,下列物质不能做该反应催化剂的是(填序号)______.
a.MnO2 b.CuSO4 c.Na2SO3 d.FeCl3
(5)W与④是相邻的同主族元素.在下表中列出H2WO3的各种不同化学性质,举例并写出相应的化学方程式.
| 编号 | 性质 | 化学方程式 |
| 示例 | 氧化性 | H2WO3+3H3PO3═3H3PO4+H2W↑ |
| 1 | ______ | ______ |
| 2 | ______ | ______ |

X溶液与Y溶液反应的离子方程式______,
N→⑥的单质的化学方程式为______冰晶石4Al+3O2↑
下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如表所示:请回答:
(1)反应①是______(填“吸热”或“放热”)反应.
(2)写出反应③的平衡常数K3的表达式______.
(3)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=______(用K1、K2表示).
(4)要使反应③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有______(填写字母序号).
A.缩小反应容器的容积 B.扩大反应容器的容积 C.升高温度
D.使用合适的催化剂 E.设法减小平衡体系中的CO的浓度
(5)若反应③的逆反应速率与时间的关系如图所示:
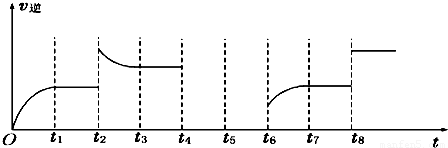
①可见反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的是什么条件:t2时______; t8时______.
②若t4时降压,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线.
0 62790 62798 62804 62808 62814 62816 62820 62826 62828 62834 62840 62844 62846 62850 62856 62858 62864 62868 62870 62874 62876 62880 62882 62884 62885 62886 62888 62889 62890 62892 62894 62898 62900 62904 62906 62910 62916 62918 62924 62928 62930 62934 62940 62946 62948 62954 62958 62960 62966 62970 62976 62984 203614
| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1173K | ||
| ①Fe(s)+CO2(g)?FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| ②Fe(s)+H2O(g)?FeO(s)+H2(g) | K2 | 2.38 | 1.67 |
| ③CO(g)+H2O(g)?CO2(g)+H2(g) | K3 | ? | ? |
(2)写出反应③的平衡常数K3的表达式______.
(3)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=______(用K1、K2表示).
(4)要使反应③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有______(填写字母序号).
A.缩小反应容器的容积 B.扩大反应容器的容积 C.升高温度
D.使用合适的催化剂 E.设法减小平衡体系中的CO的浓度
(5)若反应③的逆反应速率与时间的关系如图所示:

①可见反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的是什么条件:t2时______; t8时______.
②若t4时降压,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线.
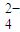 )=______mol/L.
)=______mol/L.