A、B、C、D、E、F六种元素中,除C外其他均为短周期元素,它们的原子结构或性质如下表所示:
请回答下列问题:
(1)写出A与E形成的化合物的电子式 .
(2)B的单质与D的氢化物在一定条件下反应生成BD和另一产物的化学方程式是
(3)F的盐酸盐水溶液呈酸性,原因是 (用离子方程式表示);F的单质与C、D形成的相对分子质量为160的化合物在一定条件下反应的化学方程式是
(4)化合物M是一种元素C的+6含氧酸钾盐,常用作净水剂与消毒剂.由元素C稳定的氢氧化物与次氯酸钾、氢氧化钾溶液反应制取化合物M,则制备M的离子反应方程式是 .
| 元素 | 原子结构或性质 |
| A | 原子最外层电子数是内层电子总数的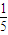 |
| B | 形成化合物种类最多的元素,其单质为固体 |
| C | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
| D | 地壳中含量最多的元素 |
| E | 与D同主族 |
| F | 与E同周期,且最外层电子数等于电子层数 |
(1)写出A与E形成的化合物的电子式 .
(2)B的单质与D的氢化物在一定条件下反应生成BD和另一产物的化学方程式是
(3)F的盐酸盐水溶液呈酸性,原因是 (用离子方程式表示);F的单质与C、D形成的相对分子质量为160的化合物在一定条件下反应的化学方程式是
(4)化合物M是一种元素C的+6含氧酸钾盐,常用作净水剂与消毒剂.由元素C稳定的氢氧化物与次氯酸钾、氢氧化钾溶液反应制取化合物M,则制备M的离子反应方程式是 .
某化学活动小组设计如图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质.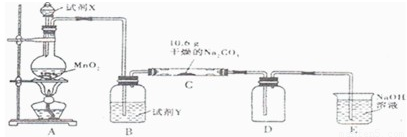
(1)写出装置A中发生反应的化学方程式: .
(2)试剂Y应选用 .
A.CCl4 B.饱和NaCl溶液 C.浓硫酸 D.饱和NaHCO3溶液
(3)通入一定量的氯气后,实验测得C中的含氯化台物只有一种,该物质属于盐类,还含有NaHCO3;D中则只有一种黄棕色的含氯氧化物,该含氯氧化物在常温下呈气态.现对C中的成分进行猜想和探究.
①提出台理假设.
假设1:存在两种成分:NaHC03和 ;假设2:存在三种成分:NaHC03和 、
②设计方案,进行实验.请写出实验步骤以及预剿现象和结论(可不填满).
限选实验试剂和仪器:蒸馏水、稀HN03、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯.
4)已知C中的Na2CO3恰好与0.1molCl2完全反应.若假设1成立,可推知C中反应的化学方程式为: .
0 62782 62790 62796 62800 62806 62808 62812 62818 62820 62826 62832 62836 62838 62842 62848 62850 62856 62860 62862 62866 62868 62872 62874 62876 62877 62878 62880 62881 62882 62884 62886 62890 62892 62896 62898 62902 62908 62910 62916 62920 62922 62926 62932 62938 62940 62946 62950 62952 62958 62962 62968 62976 203614

(1)写出装置A中发生反应的化学方程式: .
(2)试剂Y应选用 .
A.CCl4 B.饱和NaCl溶液 C.浓硫酸 D.饱和NaHCO3溶液
(3)通入一定量的氯气后,实验测得C中的含氯化台物只有一种,该物质属于盐类,还含有NaHCO3;D中则只有一种黄棕色的含氯氧化物,该含氯氧化物在常温下呈气态.现对C中的成分进行猜想和探究.
①提出台理假设.
假设1:存在两种成分:NaHC03和 ;假设2:存在三种成分:NaHC03和 、
②设计方案,进行实验.请写出实验步骤以及预剿现象和结论(可不填满).
限选实验试剂和仪器:蒸馏水、稀HN03、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯.
| 实验步骤 | 预期现象和结论 |
| 步骤l:取c中的少量固体样品于试管中,滴加足量蒸馏 水至同体溶解,然后将所得溶液分别置于a、b试管中. | |
| 步骤2: | |
| 步骤3: |
 S0
S0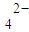 、N03-和N02-等.为确定其组成,分别进行下列4组实验,其中能确认样品中不含S0
、N03-和N02-等.为确定其组成,分别进行下列4组实验,其中能确认样品中不含S0 的实验操作是 (填下列实验操作序号);根据实验结果,你认为是否含有N02-?▲(填“含有”、“不含有”),其原因是 ;
的实验操作是 (填下列实验操作序号);根据实验结果,你认为是否含有N02-?▲(填“含有”、“不含有”),其原因是 ; 、Cl-四种离子,其中c(NH
、Cl-四种离子,其中c(NH )>c(Cl-)则这两种溶质的化学式分别是 .
)>c(Cl-)则这两种溶质的化学式分别是 .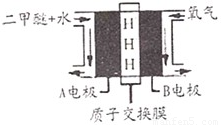


 2CuO可推出Cu+S
2CuO可推出Cu+S  CuS
CuS