碳和氮的许多化合物在工农业生产和生活中有着重要的作用.
(1)以CO2和NH3为原料可合成化肥尿素[化学式为CO(NH2)2].已知:
①2NH3(g)+CO2(g)═NH2CO2NH4(s)△H=-159kJ?mol-1
②NH2CO2NH4(S)═CO(NH2)2(s)+H2O(g)△H=1165kJ?mol-1
③H2O(l)═H2O(g)△H=44.0kJ?mol-1
则反应2NH3(g)═CO(NH2)2(s)+H2O(l)的△H=______kJ?mol-1.
(2)用活性炭原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应:
C(s)+2NO(g)?N2(g)+CO2(g)△H=QkJ?mol-1.
在T1℃时,反应进行到不同时间测得各物质的浓度如下:
①0~10min内,NO的平均反应速率v(NO)=______,T1℃时,该反应的平衡常数K=______;
②30min后,只改变某一条件,反应重新达到的平衡,根据上表中的数据判断改变的条件可能是______(填字母代号);
a.加入一定量的活性炭
b.通入一定量的NO
c.适当缩小容器的体积
d.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中,NO、N3、CO2的浓度之比为5:3:3,则Q______0(填“>”或“<”).
(1)以CO2和NH3为原料可合成化肥尿素[化学式为CO(NH2)2].已知:
①2NH3(g)+CO2(g)═NH2CO2NH4(s)△H=-159kJ?mol-1
②NH2CO2NH4(S)═CO(NH2)2(s)+H2O(g)△H=1165kJ?mol-1
③H2O(l)═H2O(g)△H=44.0kJ?mol-1
则反应2NH3(g)═CO(NH2)2(s)+H2O(l)的△H=______kJ?mol-1.
(2)用活性炭原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应:
C(s)+2NO(g)?N2(g)+CO2(g)△H=QkJ?mol-1.
在T1℃时,反应进行到不同时间测得各物质的浓度如下:
| 时间(min) 浓度(mol/L) | 10 | 20 | 30 | 40 | 50 | |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 | |
| CO2 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
②30min后,只改变某一条件,反应重新达到的平衡,根据上表中的数据判断改变的条件可能是______(填字母代号);
a.加入一定量的活性炭
b.通入一定量的NO
c.适当缩小容器的体积
d.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中,NO、N3、CO2的浓度之比为5:3:3,则Q______0(填“>”或“<”).
某化学兴趣小组的同学用如图所示实验装置进行研究,请对其方案进行完善或评价.
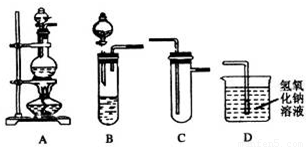
(1)浓硫酸和漂白粉可发生如下反应:
Ca(ClO)2+CaCl2+2H2SO4═2CaSO4+2Cl2↑+2H2O
实验室用此原理制取并收集氯气,可选用的装置组合是______(填写装置序号)
(2)将A、C、D相连,利用实验室常用方法制取并收集氯气.在C中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
判断实验Ⅰ、Ⅱ推出相应结论是否合理;若合理,无需填写理由,若不合理,请说明.
实验Ⅰ:______,理由______;实验Ⅱ:______,理由______;
(3)将A、C、D相连,可设计实验验证SO32-还原性强于Cl-.则C中发生反应的离子方程式是______;设计实验说明C中确实发生了上述反应(简述实验步骤、现象)______.

(1)浓硫酸和漂白粉可发生如下反应:
Ca(ClO)2+CaCl2+2H2SO4═2CaSO4+2Cl2↑+2H2O
实验室用此原理制取并收集氯气,可选用的装置组合是______(填写装置序号)
(2)将A、C、D相连,利用实验室常用方法制取并收集氯气.在C中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
| 实验 序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气体产生 | 氯气与水反应的产物具有酸性 |
实验Ⅰ:______,理由______;实验Ⅱ:______,理由______;
(3)将A、C、D相连,可设计实验验证SO32-还原性强于Cl-.则C中发生反应的离子方程式是______;设计实验说明C中确实发生了上述反应(简述实验步骤、现象)______.
有A、B、C、D四种强电解质,它们在水中电离时可产生下列离子(每种物质只含一种阴离子且互不重复,CH3COONH4溶液为中性)
已知:①A、C溶液的pH均大于7,等物质的量浓度A、B的溶液中水的电离程度相同;②C溶液和D溶液相遇时只生成白色沉淀;B溶液和C溶液相遇时只生成刺激性气味的气体;A溶液和D溶液混合时无明显现象.
(1)写出下列物质的化学式:A______,B______,C______,D______.
(2)用离子方程式表示A的水溶液显碱性的原因______.
(3)25℃时,0.1mol?L-1B溶液的pH=a,则B溶液中c(H+)-c=______(用含a的关系式表示).
(4)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序为______.
0 62656 62664 62670 62674 62680 62682 62686 62692 62694 62700 62706 62710 62712 62716 62722 62724 62730 62734 62736 62740 62742 62746 62748 62750 62751 62752 62754 62755 62756 62758 62760 62764 62766 62770 62772 62776 62782 62784 62790 62794 62796 62800 62806 62812 62814 62820 62824 62826 62832 62836 62842 62850 203614
| 阳离子 | Na+、Ba2+、NH4+ |
| 阴离子 | CH3COO-、Cl-、OH-、SO42- |
(1)写出下列物质的化学式:A______,B______,C______,D______.
(2)用离子方程式表示A的水溶液显碱性的原因______.
(3)25℃时,0.1mol?L-1B溶液的pH=a,则B溶液中c(H+)-c=______(用含a的关系式表示).
(4)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序为______.
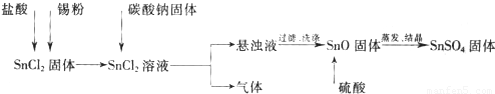
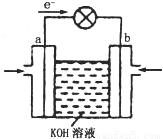
 O2(g)=CO2(g);△H=-283 kJ?mol-1
O2(g)=CO2(g);△H=-283 kJ?mol-1 2H2↑+O2↑
2H2↑+O2↑